题目内容
【题目】下列表述中一定正确的是![]()
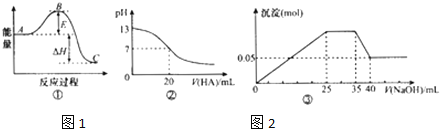
A.若图![]() 中曲线表示
中曲线表示![]() ,反应过程的能量变化.则升温或使用催化剂,均会使B点降低,反应速率加快
,反应过程的能量变化.则升温或使用催化剂,均会使B点降低,反应速率加快
B.图![]() 可表示
可表示![]() 时,用
时,用![]() 的
的![]() 溶液滴定20mL
溶液滴定20mL![]() NaOH溶液,溶液的pH随加入的酸的体积的变化情况
NaOH溶液,溶液的pH随加入的酸的体积的变化情况
C.若图![]() 表示向含
表示向含![]() 、
、![]() 、
、![]() 、
、![]() 的溶液中滴加NaOH溶液时,沉淀量随NaOH溶液加入量的变化情况,则使用的NaOH溶液的浓度为
的溶液中滴加NaOH溶液时,沉淀量随NaOH溶液加入量的变化情况,则使用的NaOH溶液的浓度为![]()
D.若图![]() 表示向含
表示向含![]() 、
、![]() 、
、![]() 、
、![]() 的溶液中滴加NaOH溶液时,沉淀量随NaOH溶液加入量的变化情况,则
的溶液中滴加NaOH溶液时,沉淀量随NaOH溶液加入量的变化情况,则![]() :
:![]()
![]() :
:![]() :3:2
:3:2
【答案】C
【解析】
A、催化加可以降低反应的活化能,加快化学反应速率,使B点降低,但是升高温度,只可以增加分子的有效碰撞,加快反应速率,不会改变活化能大小,故A错误;
B、![]() 的
的![]() 溶液和20mL
溶液和20mL![]() NaOH溶液恰好反应得到的醋酸钠溶液显示碱性,此时不会实现
NaOH溶液恰好反应得到的醋酸钠溶液显示碱性,此时不会实现![]() ,故B错误;
,故B错误;
C、反应的先后顺序:![]() 、
、![]() 结合
结合![]() 生成沉淀,
生成沉淀,![]() 与
与![]() 反应,氢氧化铝与
反应,氢氧化铝与![]() 反应而溶解,
反应而溶解,![]() ,氢氧化铝完全溶解消耗氢氧化钠5mL,
,氢氧化铝完全溶解消耗氢氧化钠5mL,![]() ,铝离子完全沉淀需要氢氧化钠15mL,所以Mg离子完全沉淀需要氢氧化钠10mL,根据镁元素守恒,镁离子物质的量是
,铝离子完全沉淀需要氢氧化钠15mL,所以Mg离子完全沉淀需要氢氧化钠10mL,根据镁元素守恒,镁离子物质的量是![]() ,消耗氢氧化钠时
,消耗氢氧化钠时![]() 即10mL,所以氢氧化钠的浓度是
即10mL,所以氢氧化钠的浓度是![]() ,故C正确;
,故C正确;
D、根据C的分析,混合物中含有镁离子的物质的量是![]() ,铝离子的物质的量是
,铝离子的物质的量是![]() ,铵根离子的物质的量是
,铵根离子的物质的量是![]() ,所以
,所以![]() :
:![]()
![]() :
:![]() :1:2,故D错误.
:1:2,故D错误.
故选C.

练习册系列答案
相关题目