题目内容
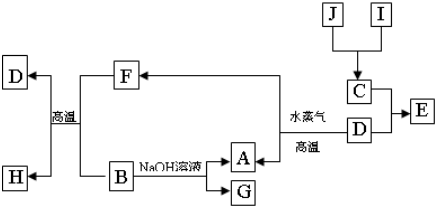
化合物X的水溶液为浅绿色,可发生如下转化关系(部分反应物、生成物略),其中B、D、E、F均为无色气体,W、K为常见金属单质,C为难溶于水的红褐固体。 在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和W反应放出大量的热。

请回答下列问题
(1)B气体的检验方法为_____________
(2)电解混合液时产生D的电极反应为______________
(3)按要求写出上述转化关系中的有关反应方程式
①含有K元素的化合反应_____________
②含有K元素的置换反应_____________
(4)K与过量G的稀溶液反应的离子方程式________________
(5)物质X的化学式____________,其水溶液的pH_____________7(填大于、小于、等于)。
(1)B气体的检验方法为_____________
(2)电解混合液时产生D的电极反应为______________
(3)按要求写出上述转化关系中的有关反应方程式
①含有K元素的化合反应_____________
②含有K元素的置换反应_____________
(4)K与过量G的稀溶液反应的离子方程式________________
(5)物质X的化学式____________,其水溶液的pH_____________7(填大于、小于、等于)。
(1)用湿润的红石蕊试纸,变蓝为NH3
(2)4OH--4e-=O2↑+2H2O
(3)①4Fe(OH)2+O2+2H2O=4Fe(OH)3
②Fe2O3+2Al 2Fe+Al2O3
2Fe+Al2O3
(4)Fe+4H++NO3-=Fe3+ +NO↑+2H2O
(5)(NH4)2Fe(SO4)2 ;小于
(2)4OH--4e-=O2↑+2H2O
(3)①4Fe(OH)2+O2+2H2O=4Fe(OH)3
②Fe2O3+2Al
 2Fe+Al2O3
2Fe+Al2O3 (4)Fe+4H++NO3-=Fe3+ +NO↑+2H2O
(5)(NH4)2Fe(SO4)2 ;小于

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
短周期元素W、X、Y、Z、在元素周期表中的位置如图所示,
| W | | | | | | | |
| | | | X | Y | Z | | |
(1)W与Z形成原子个数比为1∶1的化合物,其电子式为 。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈
酸性,其原因是 (用化学用语表示);
该溶液中各种离子浓度由大到小的顺序为 。
(3)由X W4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
。
(4)已知:2YZ2(g)
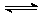 Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t
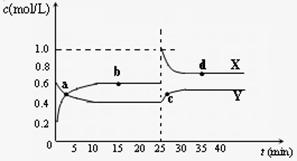 的变化关系如右图所示。
的变化关系如右图所示。① a、b、c、d四个点中,化学反应
处于平衡状态的是 点。
② 25 min时,增加了
(填物质的化学式) mol。
③ a、b、c、d四个点中所表示的反应体系
中,气体颜色由深到浅的顺序是 __
(填字母)。
短周期元素W、X、Y、Z、在元素周期表中的位置如图所示,
| W | |||||||
| X | Y | Z |
其中X、Y、Z三种元素的质子数之和为21。?
(1)W与Z形成原子个数比为1∶1的化合物,其电子式为 。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈
酸性,其原因是 (用化学用语表示);
该溶液中各种离子浓度由大到小的顺序为 。
(3)由X W4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
。
(4)已知:2YZ2(g) ![]() Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
t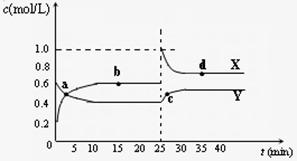 的变化关系如右图所示。
的变化关系如右图所示。
① a、b、c、d四个点中,化学反应
处于平衡状态的是 点。
② 25 min时,增加了
(填物质的化学式) mol。
③ a、b、c、d四个点中所表示的反应体系
中,气体颜色由深到浅的顺序是 __
(填字母)。


 Al(OH)3+OH-
Al(OH)3+OH- (2012?河西区二模)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.A元素的原子半径最小,与E同主族,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐X,D与E可形成淡黄色固体Y,F元素原子的最外层电子数比次外层电子数少1.请按要求回答下列问题:
(2012?河西区二模)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.A元素的原子半径最小,与E同主族,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐X,D与E可形成淡黄色固体Y,F元素原子的最外层电子数比次外层电子数少1.请按要求回答下列问题: