题目内容
将4 mol O2和3 mol NxHy(y>x)混合气体在150℃和1.05×105 Pa下点燃,完全反应后,恢复到原来的温度与压强时,测得反应后N2、O2、H2O(g)混合气体比原混合气体的密度减少3/10。(1)此反应的化学方程式是(用NxHy表示)____________________________________。
(2)推算NxHy化学式的依据是_________。
(3)x与y的关系式为__________________。
解析:(1)根据质量守恒定律可得如下化学方程式:NxHy+![]() O2====
O2====![]() N2+
N2+![]() H2O。
H2O。
(3)由题意知O2过量,则有:
4NxHy+ yO2====2xN2 + 2yH2O
4 y 2x 2y
3 mol ![]()
![]()
![]()
反应后所得气体的物质的量为(![]() ) mol。根据阿伏加德罗定律有
) mol。根据阿伏加德罗定律有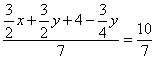 ,化简得2x+y=8。
,化简得2x+y=8。
答案:(1)4NxHy+yO2====2xN2+2yH2O
(2)质量守恒定律和阿伏加德罗定律
(3)2x+y=8

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
氨的催化氧化4NH3(g)+5O2(g) 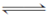 4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1是工业制备硝酸的重要反应。一定条件下将4 mol NH3和5 mol O2混合于固定容积为2 L的密闭容器中,经10 s该反应达平衡,并测得NO的浓度为0.8 mol·L-1。下列判断正确的是( )。
4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1是工业制备硝酸的重要反应。一定条件下将4 mol NH3和5 mol O2混合于固定容积为2 L的密闭容器中,经10 s该反应达平衡,并测得NO的浓度为0.8 mol·L-1。下列判断正确的是( )。
| A.以O2浓度变化表示的反应速率为0.064 mol·(L·s)-1 |
| B.反应达到平衡状态时NH3的转化率为20% |
C.升高温度能使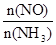 减小 减小 |
| D.将容器的体积变为4 L,平衡时NO的浓度小于0.4 mol·L-1 |

 2SO3(g)。若经过2s后测得SO3的浓度为0.6 mol/ L,用氧气表示该反应2s内的平均速率V(O2)=
;2s末O2浓度为
;2s末SO2的转化率为
。
2SO3(g)。若经过2s后测得SO3的浓度为0.6 mol/ L,用氧气表示该反应2s内的平均速率V(O2)=
;2s末O2浓度为
;2s末SO2的转化率为
。