题目内容
(8分)有机物A由碳、氢、氧三种元素组成。现取3 g A与4.48 L氧气(标准状况)在密闭容器中燃烧,生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过足量的浓硫酸和碱石灰,浓硫酸增重3.6 g,碱石灰增重4.4 g。回答下列问题:
(1)3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
【答案】
(1)n(H)= 0.4 mol n(C)=0.15mol (2)C3H8O
【解析】考查有机物分子式的计算及判断。
(1)浓硫酸和碱石灰分别吸收的是水和CO2
则n(H)=2n(H2O)=0.4 mol(2分)
n(C)=n(CO2)+n(CO)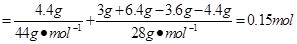 。(3分)
。(3分)
(2)3 g A中,n(H)=0.4 mol,n(C)=0.15 mo1,
n(O) =2n(CO2)+ n(CO)+ n(H2O)- 2n(O2)
=2×0.1 mol+0.05mol+0.2mol-2×0.2mol=0.05 mol
所以,n(C): n(H) :n(O)=3:8:1
即A的分子式为C3H8O。(3分)

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目




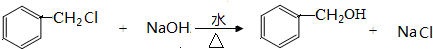
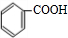 +
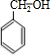
+
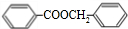 +H2O
+H2O