题目内容
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.22.4L乙烯中C-H键数为4NA
B.1.5g甲基中电子数为1.0NA
C.标准状况下,22.4L苯中含有的碳原子数为6.0NA
D.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
【答案】D
【解析】
A.没有给定标准状况下,无法计算22.4L乙烯的物质的量,无法确定C-H键的键数,选项A错误;
B.1.5g甲基为0.1mol,含有0.9mol电子,含有电子数为0.9NA,选项B错误;
C.标况下,苯不是气体,不能使用标况下的气体摩尔体积计算22.4L苯的物质的量及分子数,选项C错误;
D.乙烯和丁烯的最简式都是CH2,则n(CH2)=![]() =1.5mol,所以n(C)=1.5mol,N(C)=1.5NA,选项D正确;
=1.5mol,所以n(C)=1.5mol,N(C)=1.5NA,选项D正确;
答案选D。

【题目】消除氮氧化物和硫氧化物有多种方法。
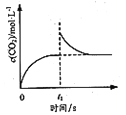
(1)用活性炭还原法:某研究小组向某密闭容器中加入足量的活性炭和NO,发生反应:C(s)+2NO(g) ![]() N2(g)+CO2(g) △H=Q kJ·mol-1 在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
N2(g)+CO2(g) △H=Q kJ·mol-1 在 T1℃下,反应进行到不同时间测得各物质的浓度部分数据如下:
时间(min) 浓度mol/L | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.40 | 0.20 | 0.30 | 0.30 | |
N2 | 0 | 0.40 | 0.60 | 0.60 | ||
CO2 | 0 | 0.60 | 0.60 |
①0~10 min 内,N2的平均反应速率 υ(N2)=________,T1℃时,该反应的平衡常数 K=_____。
②30 min 后,若只改变一个条件,反应重新达到平衡时各物质的浓度如上表所示,则改变的条件可能是____________ (填字母)
a. 加入一定量的活性炭 b. 改变反应体系的温度 c. 缩小容器的体积 d. 通入一定量的NO
③若30 min后升高温度至 T2℃,重新达到平衡时,容器中NO、N2、CO2的浓度之比为7∶3∶3,则该反应的△H______0(填“>” 、 “ =” 、或“<” )
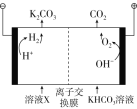
(2)NH3催化还原法:原理如图所示

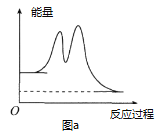
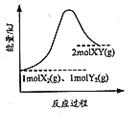
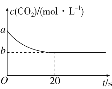
①若烟气中 c(NO2): c(NO)=1∶1,发生如图甲所示的脱氮反应时,反应过程中转移1.5mol电子时放出的热量为 113.8 kJ,则发生该脱氮反应的热化学方程式为_____ 。
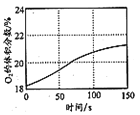
②图乙是在一定时间内,使用不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应温度分别为___;使用Mn作催化剂时,脱氮率b~a段呈现如图变化的可能原因是___。
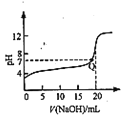
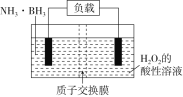
(3)直接电解吸收也是脱硝的一种方法。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如图所示。
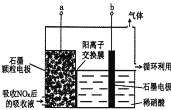
①图中b应连接电源的_________ (填“正极”或“负极”)。
②将石墨电极设置成颗粒状的目是_____________________。
③阳极的电极反应式为___________________。
【题目】有U、V、W、X、Y、Z六种前四周期元素,原子序数依次增大,其相关信息如下表:
元素编号 | 相关信息比 |
U | 所处的周期数、族序数分别与其原子序数相等 |
V | 基态时,电子分布在三个能级上,且各能级中电子数相等 |
W | 基态时, 2p 轨道处于半充满状态 |
X | 自然界中含量最多 |
Y | 是第四周期元素中未成对电子数最多的元素 |
请回答下列问题:
(1)W、X、V第一电离能由大到小顺序:________________________(用元素符号表示)
(2)V的最高价氧化物对应含氧酸中,酸根的立体构型为:_________,中心原子的杂化方式为:_______________;
(3)Y的基态原子的价电子排布图为____________________________;
(4)乙和丙分别是V和X的氢化物,这两种氢化物分子中都含有10个电子。两者沸点的关系为乙______丙(填“>”或“<”),原因是__________________________________________;
(5)V与W原子结合形成的V3W4晶体,其硬度比金刚石大,则V3W4晶体中属于____________晶体