题目内容
已知:A、B、C、D、E、F在常温下均为气体,它们有以下转化关系(部分反应条件、产物已略去).
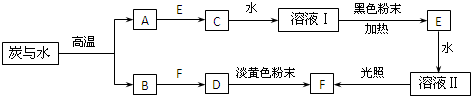
请回答下列问题:
(1)将A点燃后伸入到装有E的集气瓶中,可观察到的现象是 .
(2)C的浓溶液与黑色粉末反应生成E的化学方程式为 .
(3)若将溶液Ⅱ滴入到碘化钾溶液中,发生反应的离子方程式为 ,向反应后的溶液中加入适量CCl4,充分振荡后静置,可以观察到的现象是 .
(4)与溶液Ⅰ比较,溶液Ⅱ中多出的物质是 (填化学式).

请回答下列问题:
(1)将A点燃后伸入到装有E的集气瓶中,可观察到的现象是
(2)C的浓溶液与黑色粉末反应生成E的化学方程式为
(3)若将溶液Ⅱ滴入到碘化钾溶液中,发生反应的离子方程式为
(4)与溶液Ⅰ比较,溶液Ⅱ中多出的物质是
考点:无机物的推断,氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:炭与水在高温下生成CO与H2,B与气体F生成气体D,D与淡黄色粉末反应生成F,应是CO2与Na2O2反应生成碳酸钠与氧气,可推知B为CO,F为O2,D为CO2,故A为H2.气体E与水反应,光照可得氧气,可推知E为Cl2,溶液Ⅱ为氯水,结合转化关系可知,C为HCl,溶于水得溶液Ⅰ为盐酸,盐酸与黑色粉末二氧化锰反应可得氯气,符合转化关系,据此解答.
解答:
解:炭与水在高温下生成CO与H2,B与气体F生成气体D,D与淡黄色粉末反应生成F,应是CO2与Na2O2反应生成碳酸钠与氧气,可推知B为CO,F为O2,D为CO2,故A为H2.气体E与水反应,光照可得氧气,可推知E为Cl2,溶液Ⅱ为氯水,结合转化关系可知,C为HCl,溶于水得溶液Ⅰ为盐酸,浓盐酸与黑色粉末二氧化锰反应可得氯气,符合转化关系,
(1)将氢气点燃后伸人到装有氯气的集气瓶中,氢气在氯气中继续燃烧,发出苍白色火焰,并产生大量白雾,
故答案为:发出苍白色火焰,并产生大量白雾;
(2)浓盐酸与黑色粉末二氧化锰反应生成氯化镁、氯气与水,反应方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(3)若将氯水滴入到碘化钾溶液中,氯气氧化碘离子生成碘单质,自身被还有为氯离子,反应离子方程式为:Cl2+2I-═I2+2Cl-,
向反应后的溶液中加人适量CCl4,充分振荡后静置,萃取溶液中的碘,CCl4密度比水大,所以会看到液体分为两层,上层为无色,下层为紫红色,
故答案为:Cl2+2I-═I2+2Cl-;液体分为两层,上层为无色,下层为紫红色;
(5)与溶液I为盐酸含有:H2O、H+、Cl-,溶液Ⅱ为氯水,含有H2O、Cl2、HClO、H+、Cl-,溶液II中多出的物质是Cl2、HClO,
故答案为:Cl2、HClO.
(1)将氢气点燃后伸人到装有氯气的集气瓶中,氢气在氯气中继续燃烧,发出苍白色火焰,并产生大量白雾,
故答案为:发出苍白色火焰,并产生大量白雾;
(2)浓盐酸与黑色粉末二氧化锰反应生成氯化镁、氯气与水,反应方程式为:MnO2+4HCl(浓)
| ||
故答案为:MnO2+4HCl(浓)
| ||
(3)若将氯水滴入到碘化钾溶液中,氯气氧化碘离子生成碘单质,自身被还有为氯离子,反应离子方程式为:Cl2+2I-═I2+2Cl-,
向反应后的溶液中加人适量CCl4,充分振荡后静置,萃取溶液中的碘,CCl4密度比水大,所以会看到液体分为两层,上层为无色,下层为紫红色,
故答案为:Cl2+2I-═I2+2Cl-;液体分为两层,上层为无色,下层为紫红色;
(5)与溶液I为盐酸含有:H2O、H+、Cl-,溶液Ⅱ为氯水,含有H2O、Cl2、HClO、H+、Cl-,溶液II中多出的物质是Cl2、HClO,
故答案为:Cl2、HClO.
点评:本题考查无机物推断,侧重C、Cl、Na元素化合物转化关系考查,比较基础,注意基础知识的掌握.

练习册系列答案
相关题目
某有机物的结构简式为  .下列关于该有机物的叙述正确的是( )
.下列关于该有机物的叙述正确的是( )
 .下列关于该有机物的叙述正确的是( )
.下列关于该有机物的叙述正确的是( )| A、该有机物属于芳香烃 |
| B、该有机物苯环上一氯代物有6种 |
| C、该有机物可发生取代、加成、加聚、消去反应 |
| D、1 mol该有机物在适当条件下,最多可与3 mol Br2、5 mol H2反应 |
下列实验方案合理的是( )
| A、鉴别集气瓶中的甲烷和乙烯:移去玻璃片,分别点燃,观察火焰的颜色及是否有黑烟 |
| B、检验酒精中的少量水:向酒精中加入足量生石灰 |
| C、制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
| D、用加入浓溴水的方法分离硝基苯和苯酚的混合物 |
由铝硅两种物质组成的试样11g,均匀地分成等质量的两份,一份与足量的盐酸接触可产生气体a L,一份与足量的NaOH溶液接触产生同样的气体b L,则此试样中铝与硅的质量比为( )
A、
| ||
B、
| ||
C、
| ||
| D、无法计算 |
X、Y、Z、W为原子序数依次增大的短周期元素.其形成的小分子化合物Y2X2、Z2X4、X2W2中,分子内各原子最外层电子都满足稳定结构.下列说法正确的是( )
| A、X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X |
| B、在Y2X2、Z2X4、X2W2的一个分子中,所含的共用电子对数相等 |
| C、X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的化合物 |
| D、与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 |
下列各组中的两种物质作用,反应条件或者反应物用量改变,不会引起产物种类改变的是( )
| A、Na和O2 |
| B、NaOH和CO2 |
| C、Fe和Cl2 |
| D、AlCl3和NaOH |

 结构.
结构.
 某九年级化学活动小组同学设计了一个小游戏--物质接龙即他们之间存在着顺时针转化的关系.
某九年级化学活动小组同学设计了一个小游戏--物质接龙即他们之间存在着顺时针转化的关系.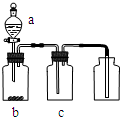 用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )