题目内容
【题目】一定条件下,物质的量均为0.3mol的X(g)与Y(g)在容积固定的密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g),ΔH=-akJ·mol-1,下列说法正确的是( )
2Z(g),ΔH=-akJ·mol-1,下列说法正确的是( )
A.反应一段时间后,X与Y的物质的量之比仍为1:1
B.达到平衡时,反应放出0.1akJ的热量
C.达到平衡后,向平衡体系中充入稀有气体,正反应速率不发生变化
D.X的体积分数保持不变,说明反应已达到平衡
【答案】C
【解析】
X(g)+3Y(g)![]() 2Z(g)
2Z(g)
初始 0.3 0.3 0
改变 x 3x 2x
平衡 0.3-x 0.3-3x 2x
A.根据三段式分析,平衡时X和Y的物质的量比不是1:1,故错误;
B.根据可逆反应的特点,各物质不能完全转化,所以有x<0.3,3x<0.3,所以有x<0.1mol,当x=0.1mol时反应放出0.1akJ的热量,故该反应实际放出的热量小于0.1akJ的热量,故错误;
C. 达到平衡后,向平衡体系中充入稀有气体,因为是固定体积,所以各物质的浓度不变,所以反应速率不变,故正确;
D.该反应中X的体积分数为![]() ,体积分数始终不变,故错误。
,体积分数始终不变,故错误。
故选C。

【题目】下列生产或实验事实引出的结论不正确的是( )
选项 | 事实 | 结论 |
A | 其他条件相同, | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 工业制硫酸过程中,在 | 增大气液接触面积,使 |
C | 在2L密闭容器中发生反应:
| 反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的 | 当其他条件不变时,催化剂可以改变化学反应速率 |
A.AB.BC.CD.D
【题目】某实验小组为探究![]() 漂白性的原因进行如下实验。已知
漂白性的原因进行如下实验。已知![]() 易溶于水,能溶于乙醇。
易溶于水,能溶于乙醇。![]() 的水溶液中存在下列平衡:
的水溶液中存在下列平衡:
![]()
![]() ;
;
![]()
![]() 。
。
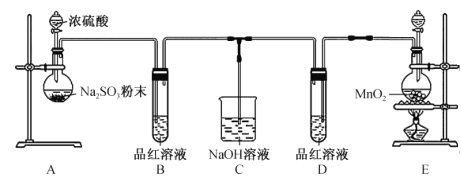
实验室用亚硫酸钠粉末与硫酸制取![]() ,装置如图
,装置如图![]() 气密性良好
气密性良好![]() 。
。

(1)盛装![]() 的硫酸的仪器名称是________。使用
的硫酸的仪器名称是________。使用![]() 的硫酸比用
的硫酸比用![]() 的硫酸反应效果好,其原因是________。装置B的作用是________。
的硫酸反应效果好,其原因是________。装置B的作用是________。
(2)第一次实验:
C装置中混合溶液 | 品红的水溶液 | 品红的乙醇溶液 |
实验现象 | 红色褪去 | 无变化 |
从上述实验可知使品红水溶液褪色的微粒可能为________![]() 写出两种即可
写出两种即可![]() 。
。
(3)实验小组为进一步探究![]() 是使品红水溶液褪色的原因之一,进行第二次实验:取与第一次实验等体积等浓度的品红水溶液于装置C中,再加入少量NaOH固体,品红水溶液无明显变化,然后通入
是使品红水溶液褪色的原因之一,进行第二次实验:取与第一次实验等体积等浓度的品红水溶液于装置C中,再加入少量NaOH固体,品红水溶液无明显变化,然后通入![]() 气体,C装置中品红水溶液褪色。以上实验______
气体,C装置中品红水溶液褪色。以上实验______![]() 填“能“或“不能”
填“能“或“不能”![]() 证明
证明![]() 是使品红溶液褪色的原因之一,试用离子方程式说明理由:________。
是使品红溶液褪色的原因之一,试用离子方程式说明理由:________。
(4)请你设计探究![]() 是使品红水溶液褪色的原因之一的实验方案:________。
是使品红水溶液褪色的原因之一的实验方案:________。