题目内容
9.草木灰中富含钾盐,主要成分是碳酸钾,还含有少量硫酸钾和氯化钾.某同学欲从草木灰中提取钾盐,并设计实验检验其中的CO32-、SO42-和Cl-,请你协助他完成实验.(1)从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③过滤,④蒸发结晶,⑤冷却结晶.
(2)用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示B.
A左盘重,样品轻 B左盘轻,砝码重 C右盘重,砝码轻 D右盘轻,样品重
(3)在进行②③④操作时,都要用到玻璃棒,其中第③步操作中玻璃棒的作用是引流,防止滤液溅到漏斗外:
(4)将制得的少量晶体放入试管,加蒸馏水溶解并把溶液分成三份,分装在三支试管里.
①在第一支试管里加入足量稀盐酸,可观察有气泡,生成,证明溶液中有CO32-离子.
②在第二支试管里加入BaCl2溶液,观察到有白色沉淀生成,该同学判断溶液中有SO42-,该同学做出的判断是否正确,并简述理由.能和氯化钡反应产生白色沉淀的可以是子或是银离子、亚硫酸根离子.
③如何确定该溶液中含有Cl-?写出简明实验方案:向原溶液中滴加足量稀硝酸后,排除了其它离子的干扰,再加入AgNO3溶液,产生白色沉淀,说明溶液中有氯离子.
分析 (1)根据从草木灰中除去不溶性的固体杂质的操作步骤分析;
(2)玻璃棒有搅拌、引流的作用;
(3)①碳酸根离子和盐酸反应产生气体;
②硫酸根离子或是银离子、亚硫酸根离子都可以和氯化钡反应生成白色沉淀;
③氯离子和硝酸酸化的银离子反应生成白色沉淀,据此回答.
解答 解;(1)从草木灰中除去不溶性的固体杂质来提取固体碳酸钾的实验操作顺序为:称量样品;溶解、沉淀;过滤;蒸发结晶.故填:蒸发结晶.
(2)在实验操作过程中,玻璃棒的作用分别是:搅拌,加速样品溶解(助溶);引流,防止滤液溅到漏斗外;搅拌(匀热),使溶液受热均匀,防止滤液飞溅.
故答案为:引流,防止滤液溅到漏斗外;
(3)①碳酸根离子能和盐酸反应生成二氧化碳,向溶液中加入稀盐酸后有气泡生成说明有碳酸根离子;故答案为:气泡;CO32-;
②向原溶液中滴加氯化钡溶液,如果产生白色沉淀,说明溶液中有硫酸根离子或是银离子、亚硫酸根离子中的一种,故答案为:否;能和氯化钡反应产生白色沉淀的可以是子或是银离子、亚硫酸根离子;
③向原溶液中滴加足量稀硝酸后,排除了其它离子的干扰,再加入 AgNO3 溶液,产生白色沉淀,说明溶液中有氯离子.
故答案为:向原溶液中滴加足量稀硝酸后,排除了其它离子的干扰,再加入 AgNO3 溶液,产生白色沉淀,说明溶液中有氯离子.
点评 本题考查了分离提纯的方法及常见阴离子的检验,难度不大,注意基础知识的积累.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
20.能用能量判断下列过程的方向的是( )
| A. | 水总是自发地由高处往低处流 | |
| B. | 有序排列的火柴散落时成为无序排列 | |
| C. | 放热反应容易进行,吸热反应不能自发进行 | |
| D. | 多次洗牌以后,扑克牌的毫无规律的混乱排列的几大 |
4.下列装置不能达到实验目的是( )


| A. | 用装置甲验证Na2O2与水的反应为放热反应 | |
| B. | 用装置乙验证铁和水蒸气的反应,方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe3O4+4H2 | |
| C. | 丙装置,将蘸取氯化钾溶液的铂丝放在酒精灯上灼烧,检验钾元素 | |
| D. | 用装置丁比较碳酸钠和碳酸氢钠的热稳定性 |
18.已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是( )
 ?
?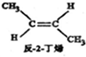 ,△H=-4.2kJ.mol-1
,△H=-4.2kJ.mol-1
 (g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
(g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
 ?
? ,△H=-4.2kJ.mol-1
,△H=-4.2kJ.mol-1 (g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.
(g)+H2(g)=CH3CH2CH2CH2(g),△=-118.9kJ.mol-1.| A. | 反-2-丁烯比顺-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热数值比反-2-丁烯小 | |
| C. | 减压和升温有利于平衡向生成正丁烷反应方向移动 | |
| D. | 反-2-丁烯氢化的热化学方程式为: (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 (g)+H2(g)?CH3CH2CH2CH3(g),△H=-123.1kJ•mol-1 |
 CuO可用作颜料、玻璃磨光剂、有机合成催化剂等.以下是用铜粉氧化法生产CuO的流程图:
CuO可用作颜料、玻璃磨光剂、有机合成催化剂等.以下是用铜粉氧化法生产CuO的流程图:
 .
. .
. +CH3OH+H2O.
+CH3OH+H2O. ,该反应类型是缩聚.
,该反应类型是缩聚. .
. 已知:2NO2(g)═N2O4(g),N2O4为无色气体.
已知:2NO2(g)═N2O4(g),N2O4为无色气体.