题目内容
将主族元素X的最高价氧化物X2O 4.7 g溶于95.3 g水中,所得溶液中溶质的质量分数为5.6%.Y与X在周期表中位于同一主族,Y的氢氧化物12 g与400 mL 0.75 moL·L-1的盐酸恰好中和.Z与Y在周期表中位于同一周期,标准状况下5.6 L ZO2气体的质量为16 g.求X、Y、Z的相对原子质量.并分别写出它们原子的电子式.
答案:
解析:
解析:
答案:X、Y、Z的相对原子质量分别为:39,23,32,电子式分别为K·,Na·,![]() .
.
思路解析:设X的相对原子质量为M(X),Y的相对原子质量为M(Y).
由

即![]() ,M(X)=39,X为钾元素;
,M(X)=39,X为钾元素;

∴![]() ,M(Y)=23,Y为钠元素;
,M(Y)=23,Y为钠元素;
ZO2的摩尔质量为![]() ×22.4 L·mol-1=64 g·mol-1,即ZO2相对分子质量为64,M(Z)=64-16×2=32,Z为硫元素.则X的相对原子质量为39,电子式为K·;Y的相对原子质量为23,电子式为Na·;Z的相对原子质量为32,电子式为
×22.4 L·mol-1=64 g·mol-1,即ZO2相对分子质量为64,M(Z)=64-16×2=32,Z为硫元素.则X的相对原子质量为39,电子式为K·;Y的相对原子质量为23,电子式为Na·;Z的相对原子质量为32,电子式为![]() .
.

练习册系列答案
相关题目
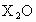 4.7g溶于95.3g水中,所得溶液
4.7g溶于95.3g水中,所得溶液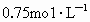 的盐酸恰好中和.Z与Y在同一周期,标准状况下5.6L
的盐酸恰好中和.Z与Y在同一周期,标准状况下5.6L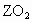 气体的质量为16g.求X、Y、Z的原子量,并分别写出它们的电子式.
气体的质量为16g.求X、Y、Z的原子量,并分别写出它们的电子式.