��Ŀ����
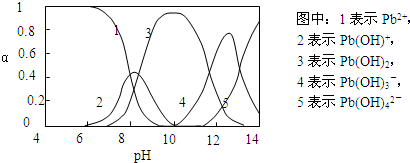
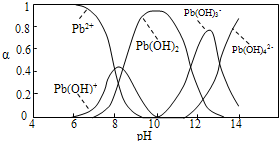
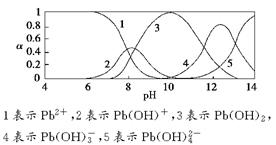
ˮ�����ؽ���Ǧ����Ⱦ���ⱸ�ܹ�ע��ˮ��Һ��Ǧ�Ĵ�����̬��Ҫ��Pb2����Pb(OH)����Pb(OH)2��Pb(OH)��Pb(OH) 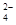 ������̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ��
������̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ��
(1)Pb(NO3)2��Һ�У�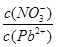 ________2(�>����������<��)��������Һ�е����Ȼ����Һ��
________2(�>����������<��)��������Һ�е����Ȼ����Һ��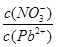 ���ӣ����ܵ�ԭ����________________________________��
���ӣ����ܵ�ԭ����________________________________��
(2)��Pb(NO3)2��Һ�е���ϡNaOH��Һ��pH��8ʱ��Һ�д��ڵ�������(Na������)��__________��pH��9ʱ��Ҫ��Ӧ�����ӷ���ʽΪ_______________________��
(3)ij�������Ʊ���һ��������Ǧ��������Чȥ��ˮ�еĺ���Ǧ��ʵ�������±���
|
�롡�� |
Pb2�� |
Ca2�� |
Fe3�� |
Mn2�� |
Cl�� |
|
����ǰŨ��/(mg��L��1) |
0.100 |
29.8 |
0.120 |
0.087 |
51.9 |
|
������Ũ��/(mg��L��1) |
0.004 |
22.6 |
0.040 |
0.053 |
49.8 |
�ϱ��г�Pb2���⣬����Ǧ�����������ӵ�ȥ��Ч����õ���________��
(4)��� ����Ǧ��(��EH��ʾ)��Ǧ��Ҫ�����ķ�Ӧ������Ϊ��2EH(s)��Pb2�� E2Pb(s)��2H������Ǧ�������pH��ΧΪ(����)
E2Pb(s)��2H������Ǧ�������pH��ΧΪ(����)
A��4��5 B��6��7 C��9��10 D��11��12
(1)>��Pb2����Cl����Ӧ��Pb2��Ũ�ȼ���
(2)Pb2����Pb(OH)����H����Pb(OH)����OH�� Pb(OH)2
Pb(OH)2
(3)Fe3����(4)B
��������������(1)��������Ǧ�Ķ��ִ��ڷ�ʽ����֪Pb2����ˮ�⣺Pb2����H2O Pb(OH)����H����Pb(OH)����H2O
Pb(OH)����H����Pb(OH)����H2O Pb(OH)2��H����������Pb(NO3)2��Һ��c(NO)/c(Pb2��)>2��������NH4Cl��Pb2����Cl����Ӧ�ȳ����Ե�PbCl2ʹPb2��Ũ�Ƚ��ͣ���c(NO)/c(Pb2��)���ӡ�(2)��������ͼʾ��֪��pH��8ʱ��Һ�д��ڵ�������ΪPb2����Pb(OH)����H��������pH��9ʱͼ��c[Pb(OH)��]Ѹ�ٽ��ͣ���Pb(OH)2Ũ�����ʷ����ķ�ӦΪPb(OH)����OH��===Pb(OH)2��(3)�����Ƚϱ����������ݿ�֪Cu2����Mn2����Cl����Ũ�ȶ����Ͳ���ԭŨ�ȵ�1/2����Fe3��ȴ����ΪԭŨ�ȵ�1/3���ʶ�Fe3����ȥ��Ч����á�(4)������ƽ���֪��Ҫʹ��ǦЧ���ã�ǦӦ��Pb2������ʽ���ڣ�pH<7����c(H��)����ʱ2EH(s)��Pb2��
Pb(OH)2��H����������Pb(NO3)2��Һ��c(NO)/c(Pb2��)>2��������NH4Cl��Pb2����Cl����Ӧ�ȳ����Ե�PbCl2ʹPb2��Ũ�Ƚ��ͣ���c(NO)/c(Pb2��)���ӡ�(2)��������ͼʾ��֪��pH��8ʱ��Һ�д��ڵ�������ΪPb2����Pb(OH)����H��������pH��9ʱͼ��c[Pb(OH)��]Ѹ�ٽ��ͣ���Pb(OH)2Ũ�����ʷ����ķ�ӦΪPb(OH)����OH��===Pb(OH)2��(3)�����Ƚϱ����������ݿ�֪Cu2����Mn2����Cl����Ũ�ȶ����Ͳ���ԭŨ�ȵ�1/2����Fe3��ȴ����ΪԭŨ�ȵ�1/3���ʶ�Fe3����ȥ��Ч����á�(4)������ƽ���֪��Ҫʹ��ǦЧ���ã�ǦӦ��Pb2������ʽ���ڣ�pH<7����c(H��)����ʱ2EH(s)��Pb2�� E2Pb(s)��2H���ֻ����淴Ӧ�����ƶ���c(H��)���˹���������Ǧ�����˵�pHΪ6��7��
E2Pb(s)��2H���ֻ����淴Ӧ�����ƶ���c(H��)���˹���������Ǧ�����˵�pHΪ6��7��
���㣺�ܹ���ȷ����ͼ������ƽ��֪ʶ����Һ�����֪ʶ���ۺ�Ӧ��
�����������ͼ������ͼ���ĺ��壬��Ӧ��ƽ��֪ʶ���⡣����η�����������ڶ��֣���Ŀ����ȥ���ӣ���ʵϸ�����У�ÿ��С�ⶼ�����dz�����֪ʶ�㡣ͼ�����Ǿ�����߿����ȵ��⡣

 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д����ǵ����Ϻ����ḻ��һ��Ԫ �أ������仯�����ڹ�ũҵ������������������Ҫ���á���ش�
�أ������仯�����ڹ�ũҵ������������������Ҫ���á���ش� ��1����һ������ĺ����ܱ������У��������»�ѧ��Ӧ�� N2(g)+3H2(g) 2NH3(g)
��1����һ������ĺ����ܱ������У��������»�ѧ��Ӧ�� N2(g)+3H2(g) 2NH3(g)
�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t/K | 298 | 398 | 498 | �� |
| K/(mol��L��1)2 | 4.1��106 | K1 | K2 | �� |
 �������⣺
�������⣺�ٱȽ�K1��K2�Ĵ�С��K1 K2���>������=����<������
���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�������� ������ţ���
A��2v(H2)������=3v(NH3)������ B��v(N2)������=3v(H2)������
C��������ѹǿ���ֲ��� D�����������ܶȱ��ֲ���
��2�������£�N2H6Cl2����һ����Ҫ�Ļ���ԭ�ϣ��������ӻ����������ˮ����Һ�����ԣ�ˮ��ԭ����NH4Cl���ơ�
��д�������µ�һ��ˮ�ⷴӦ�����ӷ���ʽ ��[��Դ:Z_xx_k.Com]
��������ˮ��Һ������Ũ
 �ȵ�����˳����ȷ���� ������ţ���
�ȵ�����˳����ȷ���� ������ţ���A��c(Cl��)>c(N2H62+)>c(H+)>c(OH��)
B��c(Cl��)>c([N2H5��H2O+])> c(H+)>c(OH��)
C��c(N2H62+)+ c([N2H5��H2O+])+c(H+)= c(Cl��)+c(OH��)
D��c(N2H62+)> c(Cl��)>c(H+)>c(OH��)
��ˮ�����ؽ���Ǧ����Ⱦ���ⱸ�ܹ�ע�������ϵ�֪Pb4+���к�ǿ�������ԡ�ˮ��Ǧ�Ĵ�����̬��Ҫ��Pb2+��Pb(OH)+��Pb(OH)2����ˮ���ܽ��С����Pb(OH)3����Pb(OH)42��������̬�����ʵ����ķ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ��
 |
��1��Pb(NO3)2��Һ�У�c(Pb2+)/c(NO3��) 1/2�����������=��������������
��2����Pb(NO3)2��Һ�μ����ᣬ��Һ��c(Pb2+)/c(NO3��)û�б������С���г������ɣ������ɵij�������Ϊ ��
��3����Pb(NO3)2��Һ�еμ�NaOH��Һ����ҺҲ����ǣ���pHԼΪ ʱ���ɳ�����࣬�����μ�NaOH��Һ�������ϵ������塣pH = 13ʱ�������ϵ�з�������Ҫ��Ӧ�����ӷ���ʽΪ��
 ��
�� ˮ�����ؽ���Ǧ����Ⱦ���ⱸ�ܹ�ע��ˮ��Һ��Ǧ�Ĵ�����̬��Ҫ��Pb2����Pb(OH)����Pb(OH)2��Pb(OH)3-��Pb(OH)42-������̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ����ͼ��ʾ��

(1)Pb(NO3)2��Һ�У� ________2(�>����������<��)��������Һ�е����Ȼ����Һ��
________2(�>����������<��)��������Һ�е����Ȼ����Һ�� ���ӣ����ܵ�ԭ����________________________________��
���ӣ����ܵ�ԭ����________________________________��
(2)��Pb(NO3)2��Һ�е���ϡNaOH��Һ��pH��8ʱ��Һ�д��ڵ�������(Na������)��__________��pH��9ʱ��Ҫ��Ӧ�����ӷ���ʽΪ_______________________��
(3)ij�������Ʊ���һ��������Ǧ��������Чȥ��ˮ�еĺ���Ǧ��ʵ�������±���
|
���� |
Pb2�� |
Ca2�� |
Fe3�� |
Mn2�� |
Cl�� |
|
����ǰŨ��/(mg��L��1) |
0.100 |
29.8 |
0.120 |
0.087 |
51.9 |
|
������Ũ��/(mg��L��1) |
0.004 |
22.6 |
0.040 |
0.053 |
49.8 |
�ϱ��г�Pb2���⣬����Ǧ�����������ӵ�ȥ��Ч����õ���________��
(4)��� ����Ǧ��(��EH��ʾ)��Ǧ��Ҫ�����ķ�Ӧ������Ϊ��2EH(s)��Pb2�� E2Pb(s)��2H������Ǧ�������pH��ΧΪ(
)
E2Pb(s)��2H������Ǧ�������pH��ΧΪ(
)
A��4��5 B��6��7 C��9��10 D��11��12

 2NH3��g��
2NH3��g��