��Ŀ����
��1������NH3������Ҫ�ĺ��������1774���������Ӣ������˹�����Ƶã�Ϊ����ʵ������ȡ����İ������ס��ҡ�����λͬѧ�ֱ��������������ʵ��װ�ã�
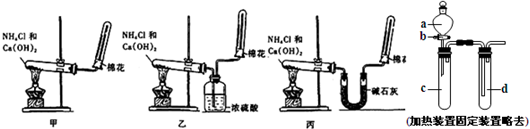
��ʵ��װ�ú�����ҩƷ����ȷ���ǣ���ס������ҡ�������______��
��д��ʵ������ȡ�����Ļ�ѧ����ʽ______��
��2��һ��ͬѧ��Ƴ���ͼ��ʾװ�������С�����Ũ���ᷴӦ��ʵ�飬��̽����ѧʵ�����ɫ����
��ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c����Ŀ����______��
����d�м�����NaOH��Һ����c�з����������м��һ������Ũ���ᣬ������Ƥ������ʱ��м����û���������ɣ�˵������Ũ�����з�����______�����Թ�c���ȣ�����ʼ�����ݲ���ʱ��Ӧ�Ļ�ѧ����ʽ��______��d�з�Ӧ�����ӷ���ʽ��______��
�⣺��1����ʵ�������Ȼ�狀����������ڼ����������Ʊ�����������Ϊ�������壬Ӧ�ü�ʯ�Ҹ���ʴ�Ϊ������
���Ȼ�狀����������ڼ������������ɰ�������Ӧ�Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2 2NH3��+CaCl2+2H2O��
2NH3��+CaCl2+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2 2NH3��+CaCl2+2H2O��
2NH3��+CaCl2+2H2O��
��2����ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c��Ŀ���Ǽ��װ�õ������ԣ��ʴ�Ϊ�����װ�������ԣ�
���������Ũ���ᷢ���ۻ����ã�����Ũ�����ڼ��ȵ������·���������ԭ��Ӧ�����������Ͷ����������壬��Ӧ�Ļ�ѧ����ʽΪ2Fe+6H2SO4��Ũ�� Fe2��SO4��3+3SO2��+6H2O�����������ж�������ֱ���ŷŵ������У�Ӧ�ü���Һ���գ���Ӧ�����ӷ���ʽΪSO2+2OH-=SO32-+H2O��
Fe2��SO4��3+3SO2��+6H2O�����������ж�������ֱ���ŷŵ������У�Ӧ�ü���Һ���գ���Ӧ�����ӷ���ʽΪSO2+2OH-=SO32-+H2O��
�ʴ�Ϊ���ۻ��� 2Fe+6H2SO4��Ũ�� Fe2��SO4��3+3SO2��+6H2O��SO2+2OH-=SO32-+H2O��
Fe2��SO4��3+3SO2��+6H2O��SO2+2OH-=SO32-+H2O��
��������1��ʵ�������Ȼ�狀����������ڼ����������Ʊ�����������Ϊ�������壬Ӧ�ü�ʯ�Ҹ��
��2����ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c��Ŀ���Ǽ��װ�õ������ԣ�
���������Ũ���ᷢ���ۻ����ã�����Ũ�����ڼ��ȵ������·���������ԭ��Ӧ�����������Ͷ����������壬���������ж�������ֱ���ŷŵ������У�Ӧ�ü���Һ���գ�
���������忼�鰱����ʵ�����Ʊ�������Ũ���ᷴӦ�����ʣ���Ŀ�ѶȲ���ע�ⳣ��Ԫ�ػ�����������Լ���ѧ����ʵ�������
���Ȼ�狀����������ڼ������������ɰ�������Ӧ�Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2
 2NH3��+CaCl2+2H2O��
2NH3��+CaCl2+2H2O���ʴ�Ϊ��2NH4Cl+Ca��OH��2
 2NH3��+CaCl2+2H2O��
2NH3��+CaCl2+2H2O����2����ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c��Ŀ���Ǽ��װ�õ������ԣ��ʴ�Ϊ�����װ�������ԣ�
���������Ũ���ᷢ���ۻ����ã�����Ũ�����ڼ��ȵ������·���������ԭ��Ӧ�����������Ͷ����������壬��Ӧ�Ļ�ѧ����ʽΪ2Fe+6H2SO4��Ũ��
 Fe2��SO4��3+3SO2��+6H2O�����������ж�������ֱ���ŷŵ������У�Ӧ�ü���Һ���գ���Ӧ�����ӷ���ʽΪSO2+2OH-=SO32-+H2O��
Fe2��SO4��3+3SO2��+6H2O�����������ж�������ֱ���ŷŵ������У�Ӧ�ü���Һ���գ���Ӧ�����ӷ���ʽΪSO2+2OH-=SO32-+H2O���ʴ�Ϊ���ۻ��� 2Fe+6H2SO4��Ũ��
 Fe2��SO4��3+3SO2��+6H2O��SO2+2OH-=SO32-+H2O��
Fe2��SO4��3+3SO2��+6H2O��SO2+2OH-=SO32-+H2O����������1��ʵ�������Ȼ�狀����������ڼ����������Ʊ�����������Ϊ�������壬Ӧ�ü�ʯ�Ҹ��
��2����ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c��Ŀ���Ǽ��װ�õ������ԣ�
���������Ũ���ᷢ���ۻ����ã�����Ũ�����ڼ��ȵ������·���������ԭ��Ӧ�����������Ͷ����������壬���������ж�������ֱ���ŷŵ������У�Ӧ�ü���Һ���գ�
���������忼�鰱����ʵ�����Ʊ�������Ũ���ᷴӦ�����ʣ���Ŀ�ѶȲ���ע�ⳣ��Ԫ�ػ�����������Լ���ѧ����ʵ�������

��ϰ��ϵ�д�
 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
�����Ŀ
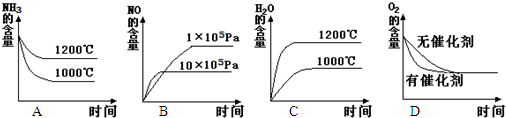
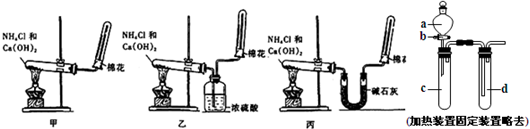

 (2) һ��ͬѧ��Ƴ���ͼ��ʾװ�������С�����Ũ���ᷴӦ��ʵ�飬��̽����ѧʵ�����ɫ����
(2) һ��ͬѧ��Ƴ���ͼ��ʾװ�������С�����Ũ���ᷴӦ��ʵ�飬��̽����ѧʵ�����ɫ����