题目内容
室温时,向0.1 mol·L-1的HAc 溶液中逐滴加入NaOH溶液,在滴加过程中,有关叙述正确的
[ ]
A. 原HAc溶液中,c(H+) = c(OH-) + c(Ac-)
B. 当滴入的NaOH与HAc恰好完全中和时,溶液中c(Na+) = c(A-),且溶液呈中性
C. 向原HAc溶液中滴入少量的0.1 mol·L-1的NaOH 溶液,可促进HAc的电离,且原溶液的pH降低
D. 当加入过量的NaOH溶液时,溶液中离子浓度可能为:c(Na+)>c(Ac-)>c(OH-)>c(H+)
B. 当滴入的NaOH与HAc恰好完全中和时,溶液中c(Na+) = c(A-),且溶液呈中性
C. 向原HAc溶液中滴入少量的0.1 mol·L-1的NaOH 溶液,可促进HAc的电离,且原溶液的pH降低
D. 当加入过量的NaOH溶液时,溶液中离子浓度可能为:c(Na+)>c(Ac-)>c(OH-)>c(H+)
AD

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
已知元素M是组成物质NH4Al(SO4)2的一种元素。元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如下表所示:
|
|
I1 |
I2 |
I3 |
I4 |
|
电离能(kJ/mol) |
578 |
1817 |
2745 |
11578 |
(1)元素M的名称是_______________;
(2)硫原子核外有______种不同运动状态的电子,有______种不同形状的电子云;
(3)请用一个事实证明氧气的氧化性比硫的氧化性强:______________________________。
(4)相同条件下,0.1 mol/L NH4Al(SO4)2中c(NH4+)________(填“等于”、“大于”或“小于”)0.1 mol/LNH4HSO4中c(NH4+)。
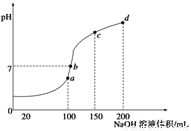
(5)室温时,向100 mL 0.1 mol/LNH4HSO4溶液中滴加0.1 mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
①试分析图中a、b、c、d四个点,水的电离程度最大的是____________;
②在b点,溶液中各离子浓度由大到小的排列顺序是________;
③在c d段发生反应的离子方程式_________________。
 M(OH)2
M(OH)2  2H++MO22-
2H++MO22- H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH 
 N2O4(g)达到平衡时NO2的体积分数
N2O4(g)达到平衡时NO2的体积分数 (NO2)随压强P的变化如图②所示,则A点的颜色深,B点的颜色浅
(NO2)随压强P的变化如图②所示,则A点的颜色深,B点的颜色浅 将增大
将增大