题目内容
17.恒温下,V升容器中加入a mol HI使之分解:2HI(g)?H2(g)+I2(g),反应达到平衡状态后,下列推测正确的是( )| A. | 减压时,v(逆)增大,v(正)减小,平衡向逆反应方向移动 | |
| B. | 若加入2a mol HI,则平衡常数变为2倍 | |
| C. | 加压时,v(逆)、v(正)均不变,平衡不移动 | |
| D. | 若保持压强不变,通入氦气,则v(逆)、v(正)均减小,平衡不移动 |
分析 A.该反应为气体体积不变的反应;
B.平衡常温与温度有关;
C.加压正逆反应速率均增大;
D.若保持压强不变,通入氦气,体积增大,相等于压强减小.
解答 解:A.该反应为气体体积不变的反应,则减压时,v(逆)减小,v(正)减小,平衡不移动,故A错误;
B.平衡常温与温度有关,则加入2a mol HI,则平衡常数不变,故B错误;
C.加压正逆反应速率均增大,平衡不移动,故C错误;
D.若保持压强不变,通入氦气,体积增大,相等于压强减小,v(逆)、v(正)均减小,平衡不移动,故D正确;
故选D.
点评 本题考查化学平衡移动,为高频考点,把握浓度、压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意化学反应的特点,题目难度不大.

练习册系列答案
相关题目
7.下列反应中,不发生氧化还原反应的是( )
| A. | 2KI+Br2═2KBr+I2 | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | NaH+H2O═NaOH+H2↑ | D. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ |
8.下表所列为五种短周期元素的相关信息:
回答下列问题:
(1)C元素在元素周期表中的位置为第二周期,第ⅤA族;
(2)B、D、E元素原子半径由大到小的顺序为Na>Al>Cl(填元素符号);
(3)A元素最高价氧化物的电子式为 ,含有的化学键类型为共价键;
,含有的化学键类型为共价键;
(4)工业上冶炼E的化学方程式为:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
(5)下列说法正确的是AD(填选项字母).
A.简单氢化物稳定性:D>A B.最高价氧化物对应水化物的酸性:A>C
C.单质的还原性:E>B D.对应离子的氧化性:E>B.
| 元素 | 元素的相关信息 |
| A | A元素存在多种同素异形体,其中一种常用电极导电材料 |
| B | 短同期中金属性最强 |
| C | 单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
| E | 地壳中含量最多的金属 |
(1)C元素在元素周期表中的位置为第二周期,第ⅤA族;
(2)B、D、E元素原子半径由大到小的顺序为Na>Al>Cl(填元素符号);
(3)A元素最高价氧化物的电子式为
 ,含有的化学键类型为共价键;
,含有的化学键类型为共价键;(4)工业上冶炼E的化学方程式为:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
(5)下列说法正确的是AD(填选项字母).
A.简单氢化物稳定性:D>A B.最高价氧化物对应水化物的酸性:A>C
C.单质的还原性:E>B D.对应离子的氧化性:E>B.
5.利用铝热反应原理可以制取锰,化学方程式为3MnO2+4Al$\frac{\underline{\;高温\;}}{\;}$3Mn+2Al2O3,该反应的氧化剂是( )
| A. | MnO2 | B. | Al | C. | Mn | D. | Al2O3 |
12.下列说法正确的是( )
| A. | NH4Cl(s)═NH3(g)+HCl(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 对于N2(g)+3H2(g)?2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率均增大 | |
| C. | 铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | |
| D. | 镀锌铁制品镀层破损后,铁制品比受损前更容易生锈,而镀锡铁则相反 |
2.胆固醇是人体必需的生物活性物质,分子式为C25H46O.已知某种胆固醇酯是液晶材料,分子式为C32H50O2.则生成这种胆固醇酯的酸是( )
| A. | C6H13COOH | B. | C6H5COOH | C. | C7H15COOH | D. | C6H5CH2COOH |
9.某物质的实验式为PtCl4•2NH3,其水溶液不导电.加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
| A. | 配合物中中心原子的电荷数为6 | B. | 该配合物可能是平面正方形结构 | ||
| C. | Cl-和NH3分子均与Pt4+形成配位 | D. | 该配合物的配体只有NH3 |
6.湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质.一种由铜镉渣生产金属镉的流程如图:
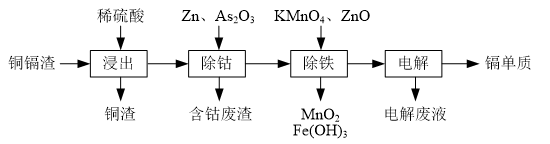
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
(1)浸出过程中,不采用通入空气的方法进行搅拌,原因是防止将Cu氧化浸出,其离子方程式是2Cu+4H++O2=2Cu2++2H2O.
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3.该微电池的正极反应式为As2O3+12H++12e-=2AsH3+3H2O.
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH.
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=1:3.
②除铁时加入ZnO控制反应液pH的范围为3.3~7.2.
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余.请设计实验方案加以验证:取样,向其中滴加H2O2后再滴入KSCN溶液,若溶液变红(或向其中滴加K3[Fe(CN)6)]溶液,若产生蓝色沉淀),则待电解液中含有Fe元素.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4.

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(2)除钴过程中,锌粉会与As2O3形成微电池产生AsH3.该微电池的正极反应式为As2O3+12H++12e-=2AsH3+3H2O.
(3)除铁时先加入适量KMnO4,再加入ZnO调节pH.
①除铁过程中,理论上参加反应的物质n(KMnO4):n(Fe2+)=1:3.
②除铁时加入ZnO控制反应液pH的范围为3.3~7.2.
(4)若上述流程中投入的KMnO4不足量,则待电解溶液中有Fe元素残余.请设计实验方案加以验证:取样,向其中滴加H2O2后再滴入KSCN溶液,若溶液变红(或向其中滴加K3[Fe(CN)6)]溶液,若产生蓝色沉淀),则待电解液中含有Fe元素.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4.
7.某元素的原子核外有3个电子层,最外层有7个电子,该原子核内的质子数为( )
| A. | 14 | B. | 15 | C. | 16 | D. | 17 |