题目内容
在周期表主族元素中,甲元素与乙、丙、丁三元素上下或左右紧密相邻,甲、乙两元素的原子序数之和等于丙元素的原子序数.这四种元素原子的最外层电子数之和为20.据此可以判断:元素甲为________,元素丙为________,元素乙和丁所形成化合物的分子式为________或________.
答案:
解析:
解析:
|
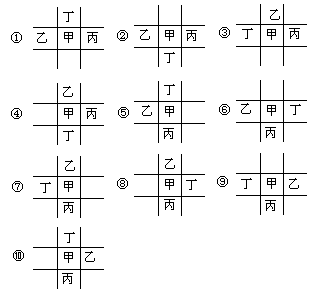
氮,磷,CO,CO2 导解:因甲与乙、丙、丁紧密相邻,且甲乙两元素原子序数之和等于丙的原子序数,则丙应在甲之后或之下,故四种元素在周期表中的位置关系可能有:
设甲最外层电子数为x,则①②③⑥⑨中有4x=20,解得x=5;而④⑤⑦⑧⑩中有4x±1=20,x不是整数,不合理.故甲最外层为5个电子为ⅤA族,此时①②③⑥中丙原子序数均不可能是乙、甲元素原子序数之和,而⑨中甲为氮,乙为氧、丙为磷、丁为碳,满足题目要求. 本题也可直接通过假设讨论求解:若丙在甲之后,则乙必为H,很显然不可能保证相邻元素最外层电子数之和为20,若丙在甲之下,则乙元素原子序数应为8,故乙为氧,由四种元素最外层电子数为20可知甲应为氮不为氟,故丙为磷,丁为碳. |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在周期表主族元素中,甲元素与乙、丙、丁三元素紧密相邻(上下或左右),甲、乙两元素的原子序数之和等于丙元素的原子序数,这四种元素原子的最外层电子数之和为20.下列说法正确的是( )
| A、甲、乙、丙、丁四种元素均为短周期元素 | B、气态氢化物的稳定性:甲>乙 | C、最高价氧化物对应的水化物的酸性:甲<丙 | D、元素丁与乙形成的化合物都是非极性分子 |