题目内容
某化学兴趣小组利用细废铁屑制取FeCl3?6H2O晶体。主要步骤如下:
①洗净后的废铁屑放在烧杯内,用过量的工业盐酸浸泡至不再产生气泡,过滤;
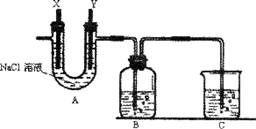
②按下图组装仪器,并检查装置的气密性,然后将①得到的滤液放入试剂瓶B中;
③将石墨电极X、Y连接上直流电源,通电,待FeCl2全部被氧化后,断开电源;
④试剂瓶B中的溶液经过一系列实验操作,可得到FeCl3?6H2O晶体。
请回答下列问题:
(1)A中的X极应连接电源的 极,
A中发生反应的化学方程式是 ;
B中溶液颜色的变化是 ;
B中反应的离子方程式是 。
(2)烧杯C中应盛放的试剂是 ,
其作用是 。
(3)试剂瓶B中的溶液由步骤④制得FeCl3?6H2O晶体,步骤④需要进行的实验操作依次是(填序号)
A.蒸发浓缩 B.洗涤 C.过滤 D.冷却结晶
(4)在整个实验过程中,盐酸必须保持过量,主要原因是
。
(1)负; ![]() ,由浅绿色变为棕黄色,
,由浅绿色变为棕黄色,
![]()
(2)NaOH溶液; 吸收Cl2
(3)A D C B
(4)抑制Fe3+水解

实验化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌.同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4?7H2O).某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾并探究其性质.
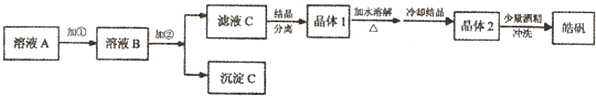
(1)制备皓矾的实验流程如图所示.

已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:
Fe(OH)3:2.7一3.7
Fe(OH)2:7.6一9.6
Zn(OH)2:5.7一8.0
试回答下列问题:①加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,应选用______,其理由是______
②加入的试剂②,供选择使用的有:Zn粉、ZnO、Zn(OH)2、ZnCO3、ZnSO4等,应选用______,其理由是______
③从晶体1→晶体2,该过程的名称是______.
④在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是______.
(2)探究ZnSO4?7H2O的性质
⑤称取28.7g ZnSO4?7H2O研细后置于坩埚中小心加热,测得残留固体的质量与温度的对应数据见下表:
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
⑥取少量ZnSO4?7H2O配成溶液向其中逐滴加入NaOH溶液,发现先产生白色沉淀后又逐渐溶解;若改用氨水得到相同的现象.查资料知,氢氧化锌与氢氧化铝均有两性,且锌离子可与氨水形成络合离子[Zn(NH3)4]2+.则Zn(OH)2沉淀中加入NaOH溶液和加氨水均得到无色溶液的离子反应方程式为:______(任写一个).