题目内容
已知Ca(OH)2在水中存在下列溶解平衡:Ca(OH)2(s)(1)写出上述两个反应的化学方程式:
①SO2与CaCO3悬浊液反应:____________________________________________________。
②SO2与Ca(OH)2悬浊液反应:________________________________________________。
(2)说明用熟石灰悬浊液而不用澄清石灰水洗涤废气的原因:_______________________。
(1)①CaCO3+SO2![]() CaSO3+CO2↑
CaSO3+CO2↑
②SO2+Ca(OH)2![]() CaSO3+H2O
CaSO3+H2O
(2)石灰水的浓度小,生成的CaSO3量小,水溶解一部分,得到产量很低

练习册系列答案
相关题目
 (2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、
(2013?江西模拟)已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、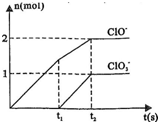 已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、
已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、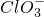 ;三种含氯元素的离子,其中C1O-、
;三种含氯元素的离子,其中C1O-、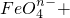 ______Cl-+______H2O.
______Cl-+______H2O.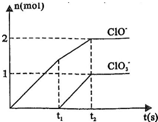
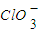 ;三种含氯元素的离子,其中C1O-、
;三种含氯元素的离子,其中C1O-、 两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
两种离子的物质的量(n)与反应时间(t)的曲线如图所示. ______Cl-+______H2O.
______Cl-+______H2O.