��Ŀ����
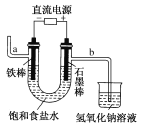
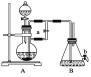
����Ŀ����ͼ��ʾװ�ã���������ȡ�۲�Fe(OH)2�ڿ����б���������ɫ�仯��ʵ��ʱ����ʹ����м��6 mol��L��1�����ᣬ�����Լ���ѡ��
��д���пհף�
(1)B��ʢ��һ������NaOH��Һ��A��ӦԤ�ȼ�����Լ���________��A�з�Ӧ�����ӷ���ʽ��___________________________��
(2)ʵ�鿪ʼʱӦ�Ƚ�����a________(�������������ر���)��
(3)��������Fe(OH)2�IJ������̣�________________________��
(4)ʵ����ϣ���b������������һ���ֿ�������ʱB�з�����Ӧ�Ļ�ѧ����ʽΪ__________________��
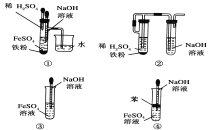
(5)��ͼ��________�ܽϳ�ʱ�俴��Fe(OH)2��ɫ������
���𰸡���1����м��Fe+2H+=Fe2++H2������2����
��3���رջ���a��������ѹǿ�������£�A�к�������������Һ��ѹ��B�У���������������������Һ��Ӧ����4��4Fe��OH��2+O2+2H2O=4Fe��OH��3����5���٢ڢۢ���
��������
��1��A��ӦԤ��ʢ�Ź�̬��Ӧ����м������ϡ���ᷴӦ�����������������������ӷ�Ӧ����ʽΪ��Fe+2H+=Fe2++H2����
��2��ʵ�鿪ʼʱ��Ӧ�ȴ�����ʹ���ɵ�������������ʵ��װ���ж��ų���������ֹ�������������������ʴ�Ϊ����
��3��A�з�Ӧ������Ϊ��֤������������B�к��������ƻ�ϣ�Ҫ��������������ѹǿ��������Ҫ�رջ���a��������ѹǿ�������£�A�к�������������Һ��ѹ��B�У���������������������Һ��Ӧ�����������ӷ�Ӧ����ʽΪ��Fe2++2OH��=Fe��OH��2��������Fe��OH��2��ɫ������
��4���������������ȶ����ױ������������ɺ��ɫ������������������ʵ����ϣ���b������������һ���ֿ��������ְ�ɫ������ת��Ϊ����ɫ���ת��Ϊ���ɫ����Ӧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��5������������Ϣ��֪Ҫ�ϳ�ʱ�䱣��Fe��OH��2��������������ȡ�����о����ܼ��ٺͿ����Ӵ����Ա��ĸ�ѡ�����Կ��Է���ѡ�������������л����������Ϳ����Ӵ��٣�����Fe��ϡ���������������ų�װ���е�����������Ҳ�ܼ����������Ӵ������ݣ�4��������Ҳ�ܼ����������Ӵ����ʴ�Ϊ���٢ڢۢ���

 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д� ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�����Ŀ���й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��CO2��ת�����л���ʵ��̼ѭ������Ч����̼�ŷš�
��1�������Ϊ1 L�ĺ����ܱ������У�����1 mol CO2��3 mol H2��һ�������·�Ӧ��CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)����H����49.0 kJmol��1�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ��ʾ��
CH3OH(g)��H2O(g)����H����49.0 kJmol��1�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ��ʾ��
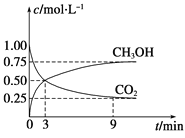
�ټ��㣺��0min��3min��H2��ƽ����Ӧ����v(H2)��_______mol��L��1��min��1����Ӧ��ƽ��ʱ���ų���������_______kJ��
����˵��������Ӧ�ﵽƽ��״̬����________(����)��
A��c(CO2) ��c(CH3OH)��1��1
B�����������ܶȲ��ٷ����仯
C����λʱ��������3mol H2��ͬʱ����1mol H2O
D��CO2����������ڻ�������б��ֲ���
�۷�Ӧ�ﵽƽ����������������䣬�ܼӿ췴Ӧ������ʹ��ϵ����������ʵ������٣��ɲ�ȡ�Ĵ�ʩ��________(����)��
A�������¶� B����С�������
C���ٳ���CO2���� D��ʹ�ú��ʵĴ���
��2����֪A(g)��B(g) ![]() C(g)��D(g) ��H����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)��D(g) ��H����Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/ �� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | x | 0.6 | 0.4 |
�ش��������⣺
�ٸ÷�Ӧ��_____��Ӧ������ȡ������ȡ�)��
��830��ʱ����һ��2L���ܱ������г���0.20mol��A��0.80mol��B����Ӧ��10sʱ�ﵽƽ�⣬���A��ת����Ϊ80%������830��ʱ����Ӧ��ƽ�ⳣ��x��____��