题目内容
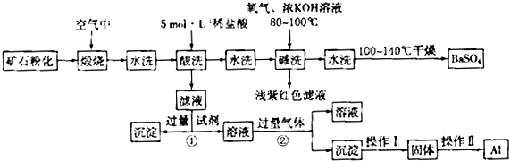
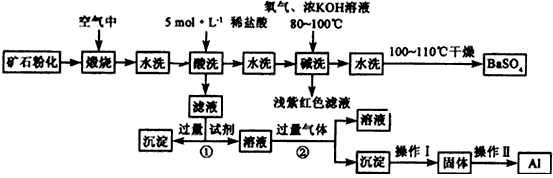
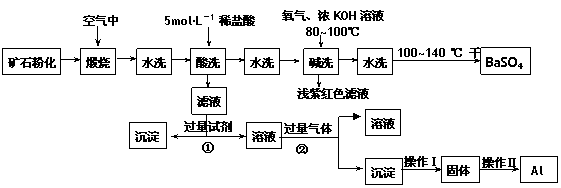
重晶石矿石主要含有BaSO4,还含有少量的SiO2、Al2O3、Fe2O3、MnO2、FeS2、Na2O、K2O等杂志.以下是某工业制备硫酸钡以及分离某些金属的流程图.
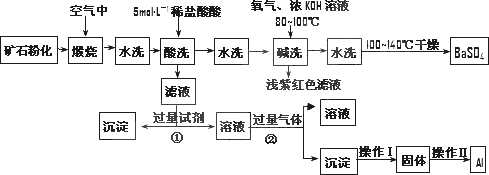
(1)煅烧过程中产生的污染性气体主要是________.
(2)确定第一次水洗液中有K+存在的实验现象是________.
(3)写出碱洗时的氧化还原反应方程式________.
(4)①反应生成沉淀的化学式________,②反应的离子方程式为________.
(5)操作Ⅰ为________ ,操作Ⅱ为________.
答案:
解析:
解析:
|
(1)SO2(1分) (2)焰色反应中透过蓝色钴玻璃观察到火焰呈紫色(2分) (3)4MnO2+3O2+4KOH (4)Fe(OH)3(1分) AlO2-+CO2+2H2O (5)加热(1分) 电解(1分) |

练习册系列答案
相关题目