题目内容
【题目】![]() 水溶液中
水溶液中![]() 、
、![]() 和
和![]() 三种形态的粒子的分布分数
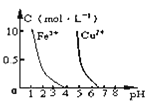
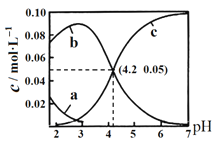
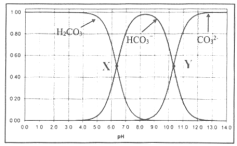
三种形态的粒子的分布分数![]() 随溶液pH变化的关系如图所示
随溶液pH变化的关系如图所示![]() 已知
已知![]() 。下列说法正确的是
。下列说法正确的是
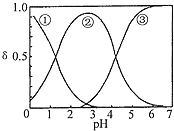
A.曲线![]() 代表的粒子是
代表的粒子是![]()
B.![]() 溶液中:
溶液中:![]()
C.![]() 时,溶液中主要含碳物质浓度大小关系为:
时,溶液中主要含碳物质浓度大小关系为:![]()
D.一定温度下,往![]() 饱和溶液中加入少量
饱和溶液中加入少量![]() 固体,
固体,![]() 将减小,
将减小,![]() 不变
不变
【答案】B
【解析】
![]() 在溶液的电离为:
在溶液的电离为:![]() ,随着pH逐渐增大,平衡右移。在此认识基础上分析图可知:粒子
,随着pH逐渐增大,平衡右移。在此认识基础上分析图可知:粒子![]() 随pH增大而减少,应为
随pH增大而减少,应为![]() ,粒子
,粒子![]() 随pH增大先减少后增多,应为
随pH增大先减少后增多,应为![]() ,粒子③随pH增大而减少,应为
,粒子③随pH增大而减少,应为![]() 。
。
A. ![]() 、
、![]() 和
和![]() 三种粒子中,只有
三种粒子中,只有![]() 随pH增大只减不增,所以曲线①代表的粒子是
随pH增大只减不增,所以曲线①代表的粒子是![]() ,故A错误;
,故A错误;
B. 由图可知![]() 溶液显示酸性,阴离子
溶液显示酸性,阴离子![]() 的电离程度大于其水解程度,所以
的电离程度大于其水解程度,所以![]() ,故B正确;
,故B正确;
C. 直接由图可看出,![]() 时,溶液中主要含碳物质浓度大小关系为:③>②>①,即
时,溶液中主要含碳物质浓度大小关系为:③>②>①,即![]() ,故C错误;
,故C错误;
D. 一定温度下,在![]() 饱和溶液中,存在
饱和溶液中,存在![]() 平衡,加入少量
平衡,加入少量![]() 固体,
固体,![]() 增大,平衡逆向移动,析出
增大,平衡逆向移动,析出![]() 固体,
固体,![]() 将减小,由于
将减小,由于![]() 不变,且溶液饱和,所以最终
不变,且溶液饱和,所以最终![]() 仍比原溶液的大,故D错误;
仍比原溶液的大,故D错误;
答案选B。

 名校课堂系列答案
名校课堂系列答案【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL。
试回答下列问题:
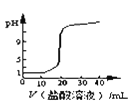
(1)锥形瓶中溶液的颜色从_________色变为___________色时,停止滴定。
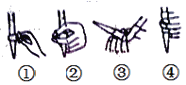
(2)下图中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是_________,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是___________(填“偏高”、“偏低”或“无影响”)
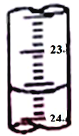
(3)图中是某次滴定时的滴定管中的液面,其读数为__________mL。
(4)根据下列数据:
滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 20.00 | 0.20 | 24.10 |
第二次 | 20.00 | 3.00 | 27.10 |
请计算待测烧碱溶液的浓度为____________mol/L。