题目内容
为测定碳酸氢钠与碳酸铵的混合物中碳酸氢钠的质量分数,李明同学从中取出18.0g,加热,使其充分反应后,测得最终残留固体质量为5.3g。
已知(NH4)2CO3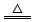 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O
(1)求原混合物中碳酸氢钠的物质的量。
(2)若将实验中生成的氨气完全溶解于10 mL水中,所得溶液的密度为0.91g/cm3,求氨水的物质的量浓度(计算结果保留一位小数)。
【答案】
(1)0.1 mol (3分)
(2)13.6 mol/L (5分)

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

