题目内容
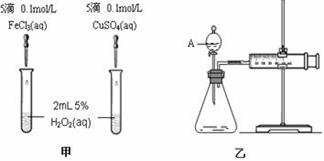
为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题

(1)定性分析:如图甲可通过观察_____________,定性比较得出结论。有同学提出将
FeCl3改为Fe2(SO4)3更为合理,其理由是_____________________,
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为__________,检查该装置气密性的方法是_____________,实验中需要测量的数据是______________。
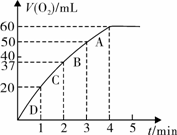
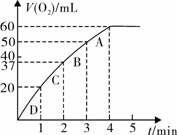
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
FeCl3改为Fe2(SO4)3更为合理,其理由是_____________________,
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为__________,检查该装置气密性的方法是_____________,实验中需要测量的数据是______________。
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①写出H2O2在二氧化锰作用下发生反应的化学方程式______________________。
②实验时放出气体的总体积是___________mL。
③放出 气体所需时间为__________min。
④反应放出 气体所需时间约为__________min。
⑤A、B、C、D各点反应速率快慢的顺序为_____>____>____>____。
⑥解释反应速率变化的原因__________。
⑦计算H2O2的初始物质的量浓度_____________。 (请保留两位有效数字)
②实验时放出气体的总体积是___________mL。
③放出 气体所需时间为__________min。
④反应放出 气体所需时间约为__________min。
⑤A、B、C、D各点反应速率快慢的顺序为_____>____>____>____。
⑥解释反应速率变化的原因__________。
⑦计算H2O2的初始物质的量浓度_____________。 (请保留两位有效数字)
(1)产生气泡的快慢;消除阴离子不同对实验的干扰
(2)分液漏斗;关闭分液漏斗的活塞,将注射器活塞向外拉出一段,过一会后看其是否回到原位;产生40mL气体所需的时间
(3)①2H2O2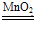 2H2O + O2↑;②60 mL; ③1 min;④2.5 min; ⑤D>C>B>A; ⑥随着反应的进行,浓度减小,反应速率减慢;⑦ 0.11 mol·L-1
2H2O + O2↑;②60 mL; ③1 min;④2.5 min; ⑤D>C>B>A; ⑥随着反应的进行,浓度减小,反应速率减慢;⑦ 0.11 mol·L-1
(2)分液漏斗;关闭分液漏斗的活塞,将注射器活塞向外拉出一段,过一会后看其是否回到原位;产生40mL气体所需的时间
(3)①2H2O2
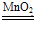 2H2O + O2↑;②60 mL; ③1 min;④2.5 min; ⑤D>C>B>A; ⑥随着反应的进行,浓度减小,反应速率减慢;⑦ 0.11 mol·L-1
2H2O + O2↑;②60 mL; ③1 min;④2.5 min; ⑤D>C>B>A; ⑥随着反应的进行,浓度减小,反应速率减慢;⑦ 0.11 mol·L-1 
练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
为比较Fe3+和Cu2+对H2O2分解的催化效果,甲、乙同学分别设计了如图一、图二所示的实验。
(1) H2O2分解的化学方程式为 。
 |
图一 图二
(2)图一所示实验能定性说明反应快慢的依据是 _______________________________;
图二所示实验能说明反应快慢的数据是____________________________________。
(3)① 用H2O2和H2SO4的混合溶液可溶解印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H= + 64.39 kJ/mol
2H2O2(l)=2H2O(l) + O2(g) △H= ﹣196. 46 kJ/mol
H2(g) + 1/2O2(g) = H2O(l) △H= ﹣285. 84 kJ/mol
在H2SO4溶液中Cu与H2O2反应生成Cu2+ 和H2O的热化学方程式为:
。
② 控制其他条件相同,印刷电路板的金属粉末用10% H2O2和3 .0 mol/L H2SO4的混
合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜平均溶解速率 (×10—3 mol·L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因
是 。