题目内容
下列离子方程式书写正确的是( )
| A、烧碱和小苏打反应:OH-+H+═H2O |
| B、氯化铁溶液腐蚀电路板:Fe3++Cu═Fe2++Cu2+ |
| C、向氢氧化钠溶液中通入足量的CO2气体:CO2+OH-═HCO3- |
| D、将硫化氢气体通入硫酸铜溶液:Cu2++S2-═CuS↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、小苏打中的碳酸氢根离子是多元弱酸根离子不能拆;
B、电子得失不守恒;
C、氢氧化钠溶液中通入足量的CO2气体生成碳酸氢根离子;
D、硫化氢是气体不能拆.
B、电子得失不守恒;
C、氢氧化钠溶液中通入足量的CO2气体生成碳酸氢根离子;
D、硫化氢是气体不能拆.
解答:
解:A、小苏打中的碳酸氢根离子是多元弱酸根离子不能拆,正确的离子方程式为OH-+HCO3-═H2O+CO32-,故A错误;
B、电子得失不守恒,正确的离子方程式为2Fe3++Cu═2Fe2++Cu2+,故B错误;
C、氢氧化钠溶液中通入足量的CO2气体生成碳酸氢根离子,离子方程式为CO2+OH-═HCO3-,故C正确;
D、硫化氢是气体不能拆,正确的离子方程式为Cu2++H2S═CuS↓+2H+,故D错误;
故选C.
B、电子得失不守恒,正确的离子方程式为2Fe3++Cu═2Fe2++Cu2+,故B错误;
C、氢氧化钠溶液中通入足量的CO2气体生成碳酸氢根离子,离子方程式为CO2+OH-═HCO3-,故C正确;
D、硫化氢是气体不能拆,正确的离子方程式为Cu2++H2S═CuS↓+2H+,故D错误;
故选C.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
设阿伏加德罗常数的值为NA,则下列说法不正确的是( )
| A、1mol氯气参加氧化还原反应时电子转移2NA |
| B、3.2g SO2与2.3g NO2所含有的氧原子数相等 |
| C、1mol Na2O2与足量水反应后转移的电子数为NA |
| D、1L0.1mol/L MgCl2溶液中Cl-离子数为0.2NA |
下列装置能构成原电池的是( )
A、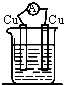 稀硫酸 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 无水乙醇 |
下列根据实验现象所得出的结论中,正确的是( )
| A、某物质焰色反应呈黄色,结论:该物质一定是钠盐 |
| B、无色试液加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝,结论:试液中一定含有NH4+ |
| C、无色溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,结论:原溶液一定含有SO42- |
| D、无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |
下列情况与平衡移动无关的是( )
| A、用KClO3制取O2时,加入少量MnO2 |
| B、滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
| C、FeCl3滴入沸水中,煮沸片刻得到红褐色胶体 |
| D、加热后的纯碱水洗油污比冷碱水效果好 |
560kg氮气与120kg氢气在一定条件下反应生成氨气,在某一时刻,体系中氢气的质量变为96kg,此时,体系中生成氨气的质量是多少( )
| A、24kg | B、68kg |
| C、136kg | D、680kg |
用下列实验装置进行的实验中,不能达到相应实验目的是( )

| A、装置甲:气体从a口进入,收集CO2 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
