��Ŀ����
|
�ݱ��������ij��˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ������ɴ�����ʹ�õ������ػ�﮵�ص�10����������ʹ��һ���²ų�һ�ε磮���ط�ӦΪ��2CH3OH��3O2��4OH�� | |
A�� |
���ʱÿ����1 mol��CH3OHת��12 mol���� |
B�� |
���ʱ��CH3OH���ɵĵ缫Ϊ���� |
C�� |
�ŵ�ʱ�������Һ��pH������ |
D�� |
�ŵ�ʱ�����ĵ缫��ӦΪ��CH3OH��8OH�� |
�𰸣�D

��ϰ��ϵ�д�
 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
�����Ŀ
 CO(g)+3H2(g) ��H
CO(g)+3H2(g) ��H  CH3OH(g) ��H
CH3OH(g) ��H 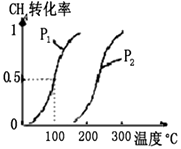
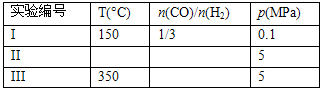
 2CO32��+ 6H2O���ŵ�ʱ�����ĵ缫��Ӧ����Ϊ_______________________
2CO32��+ 6H2O���ŵ�ʱ�����ĵ缫��Ӧ����Ϊ_______________________