题目内容
4.(1)硅及其化合物用应用广泛,光导纤维的主要成分是SiO2,工艺师在玻璃上雕刻花纹用的试剂是HF;工业上生产玻璃、水泥都要用到的原料是石灰石.高岭石的主要成分是Al2(Si2O5)(OH)4,将其化学式改写成氧化物形式是Al2O3•2SiO2•2H2O(2)氢氧化亚铁在潮湿空气中极不稳定,易被空气中氧气氧化,反应的化学方程式是_4Fe(OH)2+O2+2H2O=4Fe(OH)3;
Na2O2常用作呼吸面具或潜水艇中氧气的来源,写出Na2O2与CO2反应的化学方程式2Na2O2+2 CO2=2 Na2CO3+O2.
(3)用单线桥法标出下列氧化还原反应的电子转移数目和方向,并写出氧化剂5MnSO4+2NaClO3+4H2O═5MnO2↓+Cl2↑+Na2SO4+4H2SO4 氧化剂NaClO3
(4)酸性高猛酸钾具有强氧化性,常用作氧化剂.某反应中反应物和生成物有:MnO4-、Fe3+、H+、Mn2+、H2O和一种未知的离子X,则X离子为Fe2+.
分析 (1)光导纤维的主要成分是二氧化硅,工艺师在玻璃上雕刻花纹用的试剂是氢氟酸,工业上生产玻璃、水泥都要用到的原料是石灰石;硅酸盐由盐的书写改写为氧化物的形式即改写的一般方法归纳为:碱性氧化物、两性氧化物、酸性氧化物、水(xMO•nSiO2•mH2O);
(2)氢氧化亚铁、氧气、水反应生成氢氧化铁;Na2O2与CO2反应的化学方程式 为2Na2O2+2 CO2=2 Na2CO3+O2;
(3)5MnSO4+2NaClO3+4H2O═5MnO2↓+Cl2↑+Na2SO4+4H2SO4中,Mn元素的化合价升高,Cl元素的化合价降低,以此来解答;
(4)MnO4-→Mn2+为还原反应,Mn元素的化合价降低,则Fe元素的化合价升高.
解答 解:(1)光导纤维的主要成分是二氧化硅,工艺师在玻璃上雕刻花纹用的试剂是氢氟酸,工业上生产玻璃、水泥都要用到的原料是石灰石;硅酸盐改写成氧化物的形式为:活泼金属氧化物•较活泼金属氧化物•SiO2•H2O,同时要遵循原子守恒,故写成Al2O3•2SiO2•2H2O;
故答案为:SiO2(二氧化硅); HF(氢氟酸);石灰石;Al2O3•2SiO2•2H2O;
(2)氢氧化亚铁、氧气、水反应生成氢氧化铁,方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;Na2O2与CO2反应的化学方程式 为2Na2O2+2 CO2=2 Na2CO3+O2;故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;2Na2O2+2 CO2=2 Na2CO3+O2;
(3)5MnSO4+2NaClO3+4H2O═5MnO2↓+Cl2↑+Na2SO4+4H2SO4中,Mn元素的化合价升高,Cl元素的化合价降低,该反应转移10e-,则单线桥表示电子转移方向和数目为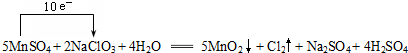 ,氧化剂为NaClO3,
,氧化剂为NaClO3,
故答案为:NaClO3;
(4)MnO4-→Mn2+为还原反应,Mn元素的化合价降低,则Fe元素的化合价升高,可知Fe2+→Fe3+为氧化反应,所以X为Fe2+,故答案为:Fe2+.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应转移电子表示方法及氧化剂判断的考查,题目难度不大.

 名校课堂系列答案
名校课堂系列答案| 选项 | 物质 | 试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 苯(苯酚) | 饱和溴水 | 过滤 |
| C | 乙烷(乙烯) | 溴水 | 洗气 |
| D | 乙烯(二氧化硫) | 酸性高锰酸钾溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 生石灰用作食品抗氧剂 | B. | 氢氧化铝用于制胃酸中和剂 | ||
| C. | 硫酸可作干燥剂 | D. | 氧化铁能用于制作吸铁石 |
| A. | 铁在氯气中燃烧,生成棕红色的烟 | |
| B. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
| A. | 浓硫酸具有吸水性,可用来干燥H2S | B. | 浓硫酸在常温下不与铁和铝反应 | ||
| C. | 可将蒸馏水注入浓硫酸进行稀释 | D. | 棉花接触浓硫酸后会变黑 |
| A. | a<b | B. | a>b | ||
| C. | c (A-)=c(Na+) | D. | 以上情况都有可能 |
| A. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 稀H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 将氢氧化铁放入盐酸中:Fe(OH)3+3H+═Fe3++3H2O |