题目内容
下列图象与文字描述正确的是( )


分析:图①体现温度对化学反应速率及化学平衡的影响,正逆反应速率相等时化学反应达到平衡状态,再升高温度,逆反应速率大于正反应速率,则化学反应逆向移动;
图②体现甲、乙达到平衡的时间不同,但反应物的含量相同,即化学平衡状态相同,则可能为催化剂或压强对反应的影响;
图③中醋酸属于弱电解质,通入氨气,生成强电解质醋酸铵,则离子的浓度增大,导电性增强;
由图④可以看出,pH为4时Fe3+完全转化为沉淀,而铜离子还没有转化为沉淀,利用铁离子水解显酸性,则可加入Cu(OH)2至溶液的pH在4左右来除杂.
图②体现甲、乙达到平衡的时间不同,但反应物的含量相同,即化学平衡状态相同,则可能为催化剂或压强对反应的影响;
图③中醋酸属于弱电解质,通入氨气,生成强电解质醋酸铵,则离子的浓度增大,导电性增强;
由图④可以看出,pH为4时Fe3+完全转化为沉淀,而铜离子还没有转化为沉淀,利用铁离子水解显酸性,则可加入Cu(OH)2至溶液的pH在4左右来除杂.
解答:解:A、由图①可知,升高温度化学平衡逆向移动,由K为生成物浓度幂之积与反应物浓度幂之积的比值,则化学反应平衡常数减小,故A错误;
B、由图②可知,可能为催化剂或压强对反应的影响,但对可逆反应2A(g)+2B(g) 3C(g)+D(s)来说,压强增大,化学平衡正向移动,反应物的含量减小,则应为催化剂对反应的影响,故B错误;
3C(g)+D(s)来说,压强增大,化学平衡正向移动,反应物的含量减小,则应为催化剂对反应的影响,故B错误;
C、因醋酸是弱电解质,醋酸与氨气反应生成醋酸铵,醋酸铵为强电解质,则溶液的导电性增强,显然与图不符合,故C错误;
D、铁离子水解显酸性,则可加入Cu(OH)2至溶液的pH在4左右,结合图可知Fe3+完全转化为沉淀,而铜离子还没有转化为沉淀,则可除去CuSO4溶液中的Fe3+,故D正确;
故选D.
B、由图②可知,可能为催化剂或压强对反应的影响,但对可逆反应2A(g)+2B(g)
 3C(g)+D(s)来说,压强增大,化学平衡正向移动,反应物的含量减小,则应为催化剂对反应的影响,故B错误;
3C(g)+D(s)来说,压强增大,化学平衡正向移动,反应物的含量减小,则应为催化剂对反应的影响,故B错误;C、因醋酸是弱电解质,醋酸与氨气反应生成醋酸铵,醋酸铵为强电解质,则溶液的导电性增强,显然与图不符合,故C错误;
D、铁离子水解显酸性,则可加入Cu(OH)2至溶液的pH在4左右,结合图可知Fe3+完全转化为沉淀,而铜离子还没有转化为沉淀,则可除去CuSO4溶液中的Fe3+,故D正确;
故选D.
点评:本题考查化学反应速率及化学平衡的图象及溶液导电、除杂等问题,考查知识点较多,注重学生对图象的分析和应用,训练了学生分析图象解决问题的能力,明确高考中对图象的考查点来解答即可.

练习册系列答案
相关题目
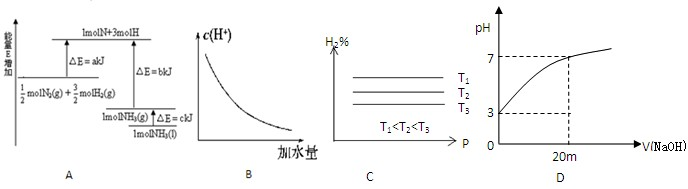

 2NH3(1)△H=-2(b+c-a)kJ?mol-1,其能量变化如图A所示
2NH3(1)△H=-2(b+c-a)kJ?mol-1,其能量变化如图A所示 2HI(g)△H<0,氢气的百分含量随温度和压强变化如图C所示
2HI(g)△H<0,氢气的百分含量随温度和压强变化如图C所示

 2AB3(g)”:升温,化学反应平衡常数增大
2AB3(g)”:升温,化学反应平衡常数增大  3C(g)+D(s)的影响且P甲<P乙
3C(g)+D(s)的影响且P甲<P乙