题目内容
8.分子式为C5H10O2的有机物能与氢氧化钠液反应生成有机盐和醇,符合条件的有机物有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
分析 分子式为C5H10O2的有机物能与氢氧化钠液反应生成有机盐和醇,说明有机物为酯,碱溶液中水解,分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,判断形成该酯的羧酸与醇的同分异构体种数.
解答 解:分子式为C5H10O2并能与NaOH溶液反应,能与氢氧化钠液反应生成有机盐和醇判断为酯,分子式为C5H10O2的酯为饱和一元酯,
①甲酸和丁醇酯化,丁醇有4种;
②乙酸和丙醇酯化,丙醇有2种;
③丙酸和乙醇酯化,丙酸有1种;
④丁酸和甲醇酯化,丁酸有2种;
因此属于酯的共4+2+1+2=9种,
因此符合条件的C5H10O2的同分异构体共9种,
故选D.
点评 本题主要考查同分异构体书写、官能团的性质与确定等,题目难度中等,掌握有机物的性质和同分异构体的书写规则是关键.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
18.甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,片刻沉淀由白色变为灰绿色又变为红褐色;将丁溶液滴入甲溶液,有白色沉淀生成,而将甲溶液滴入丁溶液时,无沉淀生成,据此可推断丙物质是( )
| A. | Al2(SO4)3 | B. | BaCl2 | C. | NaOH | D. | FeSO4 |
19.下列各组离子在碱性条件下可以大量共存,在酸性条件下因发生氧化还原反应而不能大量共存的是( )
| A. | Cu2+ Fe2+ NO3- Cl- | B. | K+ Mg2+HCO3-SO42- | ||
| C. | S2- Na+ K+、Cl- | D. | Ba2+Na+ I- NO3- |
16.下列说法正确的是( )
| A. | 钢铁发生电化腐蚀的负极反应式:Fe-3e-═Fe3+ | |
| B. | 氢氧燃料电池的正极反应式:O2+2H2O+4e-═4OH- | |
| C. | 铜上镀锌时,与电源正极相连的是纯铜 | |
| D. | 用惰性电极电解饱和食盐水时,阴极的电极反应式为:2Cl--2e-═Cl2↑ |
13.某烃的一种同分异构体只有一种一氯代物,则该烃的分子式可以是 ( )
| A. | C5H12 | B. | C6H14 | C. | C4H10 | D. | C7H16 |
20.在标准状况下,下列物质所占体积最大的是( )
| A. | 98gH2SO4 | B. | 56gFe | C. | 44.8LHCI | D. | 6gH2 |
2.工业上制备乙酸正丁酯有关化合物的物理性质见表:
已知:乙酸正丁酯、正丁醇和水组成三元共沸物恒沸点为90.7℃.
(一)合成:
方案甲:采用装置甲,在烧瓶中加入11.5mL正丁醇、7.2mL冰醋酸、3~4滴浓硫酸和沸石,摇匀.安装好带分水器的回流反应装置,通冷却水,加热.在反应过程中通过分水器下部的旋塞分出生成的水.反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.

(二)提纯:甲乙两方案提纯方法均如下:

回答下列问题:
(1)a处水流方向是进水(填“进水”或“出水”),仪器b的名称(直形)冷凝管.
(2)合成步骤中,判断方案甲酯化反应已基本完成的标志是分水器中水不再生成或分水器中的水层不再增加时.
(3)提纯过程中,步骤②是为了除去有机层中残留的酸,检验有机层已呈中性的操作是用玻璃棒蘸取有机层,点在pH试纸上,与标准比色卡对照,读取pH值判断;步骤③的目的是除去溶于酯中的少量无机盐.
(4)下列有关洗涤过程中分液漏斗的使用正确的是BC(选填序号).
a.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
b.洗涤时振摇放气操作应如图戊所示
c.放出下层液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
d.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验中乙酸丁酯产率较高的方案是方案甲,理由是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
(一)合成:
方案甲:采用装置甲,在烧瓶中加入11.5mL正丁醇、7.2mL冰醋酸、3~4滴浓硫酸和沸石,摇匀.安装好带分水器的回流反应装置,通冷却水,加热.在反应过程中通过分水器下部的旋塞分出生成的水.反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.

(二)提纯:甲乙两方案提纯方法均如下:

回答下列问题:
(1)a处水流方向是进水(填“进水”或“出水”),仪器b的名称(直形)冷凝管.
(2)合成步骤中,判断方案甲酯化反应已基本完成的标志是分水器中水不再生成或分水器中的水层不再增加时.
(3)提纯过程中,步骤②是为了除去有机层中残留的酸,检验有机层已呈中性的操作是用玻璃棒蘸取有机层,点在pH试纸上,与标准比色卡对照,读取pH值判断;步骤③的目的是除去溶于酯中的少量无机盐.
(4)下列有关洗涤过程中分液漏斗的使用正确的是BC(选填序号).
a.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
b.洗涤时振摇放气操作应如图戊所示
c.放出下层液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
d.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验中乙酸丁酯产率较高的方案是方案甲,理由是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
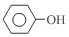 +3Br2→
+3Br2→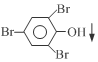 +3HBr
+3HBr