题目内容
将0.l mol·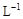 氨水溶液加水稀释,下列说法正确的是
氨水溶液加水稀释,下列说法正确的是
| A.溶液中c(H+)和c(OH-)都减小 | B.溶液中c(OH-)增大 |
| C.NH3·H2O电离平衡向左移动 | D.溶液的pH减小 |
D
解析试题分析:A、因醋酸溶液中加水稀释,溶液的体积增大,则电离产生的氢离子的浓度减小,则氢氧根浓度增大,故A错误;
B、因醋酸溶液中加水稀释,溶液的体积增大,则电离产生的氢离子的浓度减小,故B错误;
C、醋酸是弱电解质,则醋酸溶液中加水稀释将促进电离,平衡向右移动,故C错误;
D、醋酸溶液中加水稀释,溶液的体积增大,则电离产生的氢离子的浓度减小,根据Kw值不变,所以氢氧根浓度增大,故D正确;
故选D。
考点:弱电解质在水溶液中的电离平衡
点评:本题考查弱电解质的稀释,明确温度与电离平衡常数的关系、溶液的pH与物质的量浓度的关系、稀释中溶液体积的变化与离子的物质的量的变化程度是解答本题的关键。

练习册系列答案
相关题目
|
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是 | |
A. |
将0.1 mol氨充分溶解在1 L水中 |
B. |
将10 g质量分数为98%的硫酸与990 g水混合 |
C. |
将8 g三氧化硫溶于水并配成1 L溶液 |
D. |
将0.1 mol氧化钠溶于水并配成1 L溶液 |