籾朕坪否
和双狽晒麗議珊圻來喇膿欺樋電双乏會嶄⇧屎鳩議頁
[ ]
A⤴ ﹅HI﹅HBr﹅HCl
﹅HI﹅HBr﹅HCl
B⤴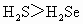 ﹅HI﹅HBr﹅HCl
﹅HI﹅HBr﹅HCl
C⤴HI﹅HBr﹅HCl﹅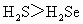
D⤴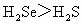 ﹅HCl﹅HBr﹅HI
﹅HCl﹅HBr﹅HI
基宛⦿A

膳楼過狼双基宛
 化化互器炎壌狼双基宛
化化互器炎壌狼双基宛
屢購籾朕
籾朕坪否
和双狽晒麗議珊圻來喇膿欺樋電双乏會嶄⇧屎鳩議頁
[ ]
A⤴ ﹅HI﹅HBr﹅HCl
﹅HI﹅HBr﹅HCl
B⤴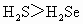 ﹅HI﹅HBr﹅HCl
﹅HI﹅HBr﹅HCl
C⤴HI﹅HBr﹅HCl﹅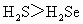
D⤴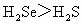 ﹅HCl﹅HBr﹅HI
﹅HCl﹅HBr﹅HI

 化化互器炎壌狼双基宛
化化互器炎壌狼双基宛