题目内容
金属锡的纯度可以通过下述方法分析测定,将试样溶于盐酸,溶液中再加入过量的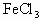 溶液,
溶液,
反应为![]() ,最后用
,最后用![]() 反应,
反应,
反应式为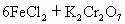 +14HCl→
+14HCl→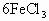 +2KCl+
+2KCl+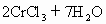 ,现有0.613g金属锡样品经上述各步反应后共用去16mL0.100mol/L
,现有0.613g金属锡样品经上述各步反应后共用去16mL0.100mol/L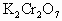 溶液,求该样品中锡的质量分数.
溶液,求该样品中锡的质量分数.
答案:
解析:
解析:
|
设样品中含锡的质量为x 解:Sn+2HCl→ x=0.571 g 所以样品含锡的质量分数为: |

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
 ↑
↑
 +14HCl→
+14HCl→ +2KCl+
+2KCl+

 ×100%=93.1%.
×100%=93.1%.