题目内容
15.下列说法正确的是( )①最外层电子数是2的元素一定是金属元素
②元素周期表中,非金属性最强的元素是F
③盐酸是强酸,H2S是弱酸,故非金属性:Cl>S
④X元素的阳离子和Y元素的阴离子具有相同的电子层结构,则原子序数:X>Y
⑤O2和O3属于同素异形体,故它们的性质相同.
| A. | ①④ | B. | ①③⑤ | C. | ①②④ | D. | ②④ |
分析 ①最外层电子数是2的元素有He、第ⅡA族元素、某些过渡元素;
②元素周期表中,右上角元素的非金属性最强;
③不能利用无氧酸的酸性比较其非金属性;
④X元素的阳离子和Y元素的阴离子具有相同的电子层结构,则X在Y的下一周期;
⑤O2和O3属于同素异形体,为不同的单质.
解答 解:①最外层电子数是2的元素有He、第ⅡA族元素、某些过渡元素,则最外层电子数是2的元素可能为He,故错误;
②元素周期表中,右上角元素的非金属性最强,即F的非金属性最强,故正确;
③不能利用无氧酸的酸性比较其非金属性,则盐酸是强酸,H2S是弱酸,但不能比较Cl、S的非金属性,故错误;
④X元素的阳离子和Y元素的阴离子具有相同的电子层结构,则X在Y的下一周期,可知原子序数:X>Y,故正确;
⑤O2和O3属于同素异形体,为不同的单质,则性质不同,故错误;
故选D.
点评 本题考查元素周期表及元素周期律的综合应用,为高频考点,把握原子结构、元素的位置和性质、元素周期律等为解答该题的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列关于甲烷的说法正确的是( )
| A. | 能使溴的四氯化碳溶液褪色 | B. | 是天然气的主要成分 | ||
| C. | 不能发生燃烧反应 | D. | 能发生加成反应 |
3.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 常温下,0.1mol/L NH4NO3溶液中NO3-的数目为0.1NA | |
| C. | 标准状况下,11.2L CCl4中含有分子的数目为0.5NA | |
| D. | 室温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
10.某学习小组为探究原电池工作原理,设计如图装置,下列叙述不正确的是( )
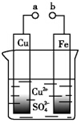

| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铁片上发生的反应为:Cu2++2e Cu Cu | |
| C. | a和b用导线连接时,Fe为负极,Cu为正极,化学能转化为电能 | |
| D. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 |
7.NA表示阿伏加德罗常数的值.下列说法不正确的是( )
| A. | 0.5mol H2O中含有的原子总数为1.5 NA | |
| B. | 0.2mol O2 所占有的体积为4.48L | |
| C. | 22g 二氧化碳气体中所含有的分子数目为0.5 NA | |
| D. | 100mL2mol/L的Na2CO3溶液中含有的Na+数目为0.4NA |
1.下列各组物质的溶液混合,如果其中酸过量时,仍有沉淀生成的是( )
| A. | NaOH、FeCl3、H2SO4 | B. | HCl、K2CO3、BaCl2 | ||
| C. | CuSO4、HCl、KOH | D. | BaCl2、HNO3、AgNO3 |
 如图为相互串联的甲乙两个电解池,甲池若为电解精炼铜的装置,请回答:
如图为相互串联的甲乙两个电解池,甲池若为电解精炼铜的装置,请回答: