��Ŀ����

��2��Ԫ�آ�����γɵĻ�����ľ���������_____________��
��3��Ԫ�آܵĵ�һ������_________ ���>������=����<����Ԫ�آݵĵ�һ�����ܣ�Ԫ�آ���Ԫ�آ� �γɵ�X���ӵĿռ乹��Ϊ_________��X�е����ͬ������Ԫ����Ԫ�آ��γɵĻ�����ķе㣬��ԭ����________________________��
��4��������������Ԫ�صĻ�̬ԭ���У�4p������������_________������Ԫ�ط��ţ���ͬ����3d����������ԭ����_______��4s������������_______��
��5����������Xͨ�뺬��Ԫ�آ����ɫ��������Һ�У������ӷ���ʽΪ______________��

��2�����Ӿ���
��3��>�� �����Σ�X���Ӽ����γ����
��4��As��Cr��Mn��K��Cr��Cu
��5��4NH3 + Cu2+=Cu(NH3)42+

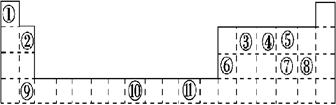
��2011?������ģ��X��Y��Z��W��Ϊ����������Ԫ�أ�X��W��������֮��Ϊ23���±�Ϊ���ڱ���һ���֣�����˵����ȷ���ǣ�������
|
��13�֣��±�Ϊ���ڱ���һ���֣��������е���ĸ�ֱ����һ�ֻ�ѧԪ�ء�
|
a |
|
|
|
|
|||||||||||||
|
|
|
|
|
b |
c |
d |
|
|
|||||||||
|
|
|
|
|
|
e |
f |
|
|
|||||||||
|
|
|
|
|
|
g |
|
h |
|
|
|
|
|
|
|
|
|
|
�û�ѧ����ش��������⣺
��1��д��Ԫ��g�Ļ�̬ԭ�Ӻ�������Ų�ʽ___________________________��
h2+��δ�ɶԵ�����Ϊ ��
��2����b2a2�����У�Ԫ��bΪ �ӻ����÷����� ���ӣ�����ԡ��Ǽ��ԡ������÷����ЦҼ��ͦм�����Ŀ��Ϊ ��
��3�� bd2��bf2�Ƚϣ��е�ϸߵ���_______�������ʽ����ԭ���� ��
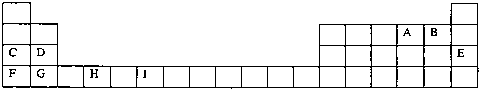
��4�����й���Ԫ����Ԫ�����ڱ��е�λ���Լ�Ԫ��ԭ�ӵ���Χ�����Ų��ص���й�����ȷ�� ��
A��hλ��Ԫ�����ڱ��е������ڵ�VIII�壬����d��Ԫ��
B��e�Ļ�̬ԭ���У�3p�ܼ�Ϊ�����������p��Ԫ��
C�����������Ų�ʽΪ4s2��һ������IIA��
D�����������Ų�ʽΪns2np1����Ԫ�ؿ����Ǣ�A����B��
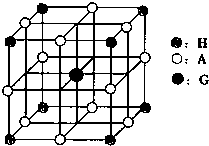
��5����ѧ�о�������Ԫ��b��Ԫ��c�����γ�һ�ֳ�Ӳ����ĥ�����µ��������ǽ������ϣ��仯ѧʽΪ �����۵�Ƚ��ʯ ����ߡ��͡�����


 ��۵����Ų�ʽ__________�����������е����Ų�4s����ϵ�������֮��ͬ�Ļ��� Ԫ��(��Ԫ�ط���)��
��۵����Ų�ʽ__________�����������е����Ų�4s����ϵ�������֮��ͬ�Ļ��� Ԫ��(��Ԫ�ط���)��