题目内容
12. 利用Fe+CuSO4=Cu+FeSO4设计一个原电池.画出实验装置图. 并指出:
利用Fe+CuSO4=Cu+FeSO4设计一个原电池.画出实验装置图. 并指出:正极为Cu(或C等),电极反应:Cu2++2e-=Cu;
负极为Fe,电极反应:Fe-2e-=Fe2+.
分析 根据原电池工作原理结合总反应方程式,还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液,由此分析解答.
解答 解:不如负极活泼的金属或导电的分金属作正极,根据反应方程式,可选铜作正极,正极上铜离子得电子生成铜单质,电极反应式为:Cu2++2e-═Cu,而CuSO4+Fe═FeSO4+Cu,该反应中,铁失电子生成二价铁离子进入溶液,所以铁作还原剂,电极反应式为:Fe-2e-═Fe2+;实验装置图为: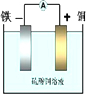 ,
,
故答案为:Cu(或C等),Cu2++2e-=Cu;Fe; Fe-2e-=Fe2+.
点评 本题考查了原电池的设计,原电池的设计关键是负极材料和电解质溶液的成分,一般来说,还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液.

练习册系列答案
相关题目
2.下列配合物的配位数不是6的是( )
| A. | K2[Co(SCN)4] | B. | Na2[SiF6] | C. | Na3[AlF6] | D. | [Cu(NH3)4]Cl2 |
3.下列说法正确的是( )
| A. | 离子化合物中一定不含共价键 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | 两种元素组成的化合物中一定不含非极性键 | |
| D. | 氢键只存在于分子之间 |
20.澳大利亚研究人员最近开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫碳”,它外形类似海绵,密度极小,并具有磁性.纳米泡沫碳与金刚石的关系是( )
| A. | 同分异构体 | B. | 不同密度的核素 | C. | 同位素 | D. | 同素异形体 |
7.已知自然界氧的同位素有16O、17O、18O,水中氢的同位素有H、D,从水分子的原子组成来看,自然界的水分子可以有( )
| A. | 3种 | B. | 6种 | C. | 9 种 | D. | 12种 |
17.相同温度下,相同物质的量浓度的四种溶液:①CH3COONa,②NH4Cl,③NaHCO3,④Na2CO3.按pH值由大到小顺序排列正确的是( )
| A. | ④①③② | B. | ①④③② | C. | ①②③④ | D. | ④③①② |
4.下列有关有机物 的性质叙述不正确的是( )
的性质叙述不正确的是( )
 的性质叙述不正确的是( )
的性质叙述不正确的是( )| A. | 能使溴水褪色 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 能发生加成反应 | |
| D. | 能发生加聚反应,且生成的聚合物也能使溴水褪色 |
1.下列说法正确的是( )
| A. | 增大反应物的量,化学反应速率一定加快 | |
| B. | 气体反应体系的压强增大,化学反应速率一定加快 | |
| C. | 与金属锌反应时,硫酸的浓度越大,产生H2速率越快 | |
| D. | 2molX气体在2L的容器中反应,4s后浓度变为0.5mol•L-1,则其反应速率为0.125mol•L-1•s-1 |
 .
.