题目内容
已知A是由甲、乙两种常见金属元素形成的单质组成的混合物,有如下转换关系。回答下列问题: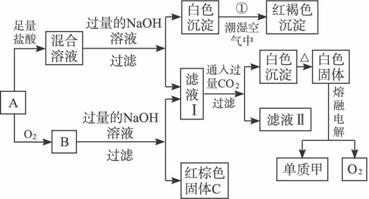
(1)单质乙的化学式为_________________________________________________。
(2)单质甲与红棕色固体在高温下反应的化学方程式_______________________________。
(3)反应①的化学方程式_________________________________________________。
(4)若向滤液Ⅰ中加入过量的盐酸,写出有关反应的离子方程式_____________________。
(5)向20 mL浓度为1 mol/L的甲的氯化物水溶液中加入1 mol/L的NaOH溶液,生成沉淀
(1)Fe
(2)2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
(3)4Fe(OH)2+O2+2H2O====4Fe(OH)3
(4)![]() +4H+====Al3++2H2O
+4H+====Al3++2H2O
(5)30 mL、70 mL
解:红褐色沉淀为Fe(OH)3,由反应①知白色沉淀为Fe(OH)2,说明A中有单质Fe,A与O2反应有两种氧化物,但加入NaOH溶液后只得红棕色固体C(Fe2O3),那么,另一种氧化物能与NaOH溶液反应,易知为Al2O3,则A中有单质Al,Ⅰ为NaAlO2,向NaAlO2溶液中通入过量CO2生成Al(OH)3沉淀和NaHCO3,即Ⅱ为NaHCO3。由2Al2O3(熔融)![]() 4Al+3O2↑知甲为Al,乙为Fe。Al与Fe2O3反应为铝热反应,即Fe2O3+2Al
4Al+3O2↑知甲为Al,乙为Fe。Al与Fe2O3反应为铝热反应,即Fe2O3+2Al![]() Al2O3 +2Fe。对第(5)问,若NaOH少量,Al3+过量,由关系式3OH-—Al(OH)3↓知V(NaOH)=30 mL;若NaOH的量较多,Al3+完全反应,则反应有Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-====
Al2O3 +2Fe。对第(5)问,若NaOH少量,Al3+过量,由关系式3OH-—Al(OH)3↓知V(NaOH)=30 mL;若NaOH的量较多,Al3+完全反应,则反应有Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-====![]() +2H2O(生成的沉淀部分溶解,剩余
+2H2O(生成的沉淀部分溶解,剩余