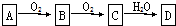题目内容
19.如图是某硫酸试剂瓶的标签上的部分信息.下列说法正确的是( )
| A. | 常温下,该试剂可与金属铝反应生成大量的无色气体 | |
| B. | 1mol Zn与足量的该硫酸反应生成2g氢气 | |
| C. | 该硫酸与等体积水混合所得溶液的物质的量浓度大于9.2mol/L | |
| D. | 向50mL该硫酸中加入足量的铜片,加热,反应后被还原的硫酸的物质的量等于0.46mol |
分析 A.浓硫酸具有强的氧化性,能够使铝钝化;
B.浓硫酸具有强氧化性,与活泼金属反应不生成氢气;
C.该硫酸与水的密度不同,混合所得溶液的总体积不等于硫酸体积的二倍;
D.铜只与浓硫酸反应,与稀硫酸不反应.
解答 解:A.浓硫酸具有强的氧化性,能够使铝钝化,阻止反应进行,故A错误;
B.锌与浓硫酸反应生成硫酸锌、二氧化硫和水,故B错误;
C.硫酸与等体积水混合后,所得溶液中硫酸的物质的量不变,则稀释前后,硫酸的物质的量不变,C1V1=C2V2,所以C2=$\frac{{C}_{1}{V}_{1}}{{V}_{2}}$=$\frac{18.4{V}_{1}}{{V}_{2}}$,但是V2<2V1,所以所得溶液的物质的量浓度大于9.2mol/L,故C正确;
D.50mL该硫酸中加入足量的铜片,若硫酸完全反应则被还原的硫酸的物质的量等于0.46mol,但是因为硫酸定量,随着反应进行,硫酸不断消耗,浓度降低变为稀硫酸,稀硫酸不能与铜反应,所以被还原的硫酸的物质的量小于0.46mol,故D错误;
故选:C.
点评 本题考查了浓硫酸的性质,熟悉浓硫酸的强氧化性是解题关键,注意钝化反应属于化学变化,题目难度不大.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
9.正确的实验操作是实验成功的重要因素,下列实验操作正确的是( )
| A. | 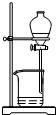 放出碘的苯溶液 放出碘的苯溶液 | B. | 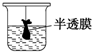 分离或提纯胶体 分离或提纯胶体 | ||
| C. | 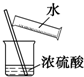 实验室稀释浓硫酸 实验室稀释浓硫酸 | D. | 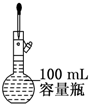 定容 定容 |
11.下列说法不正确的是( )
| A. | 增大压强,单位体积内活化分子数目不变,化学反应速率增大 | |
| B. | 升高温度,活化分子数目增大,化学反应速率增大 | |
| C. | 加入反应物,单位体积内活化分子数目增大,化学反应速率增大 | |
| D. | 使用催化剂,单位体积内活化分子数目增大,化学反应速率增大 |
8.下列实验方法或操作不正确的是( )
| A. | 检验某溶液中是否含有Fe3+时,可滴加硫氰化钾溶液,若溶液由无色变为血红色,则说明溶液中一定含有Fe3+ | |
| B. | 稀释浓硫酸时要将水沿烧杯内壁慢慢注入浓硫酸中 | |
| C. | 用CCl4萃取碘水后分液时,先打开分液漏斗活塞,放出下层液体,再关闭活塞,从漏斗上口倒出上层液体 | |
| D. | 热的纯碱溶液可用于除油污 |
9.下列说法正确的是( )
| A. | 试管、烧杯、表面皿、蒸发皿、圆底烧瓶都能用酒精灯直接加热 | |
| B. | 实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗 | |
| C. | 通常用产生气泡的快慢,比较不同条件下Na2S2O3溶液与稀硫酸反应速率 | |
| D. | 当振荡分液漏斗中的混合溶液时,用右手压住分液漏斗的玻璃塞,左手握住旋塞,上下用力振荡 |