题目内容
【题目】25℃时,用已知浓度的NaOH溶液滴定某浓度的弱酸 HA,其滴定曲线如图所示,下列说法正确的是
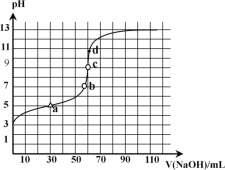
A.滴定时,可用酚酞作指示剂
B.a点表示反应终点
C.在b点时:c(Na+)=c(A-)
D.在c点时:c(A-)>c(Na+)>c(OH-)>c(H+)
【答案】AC
【解析】
A. 滴定终点是NaA溶液,溶液水解显碱性,因此滴定时,可用酚酞作指示剂,故A正确;
B. 根据氢氧化钠滴定弱酸HA恰好反应生成NaA,NaA水溶液水解显碱性,终点是碱性,而a点溶液呈酸性,故B错误;
C. 在b点时根据电荷守恒c(Na+) +c(H+) =c(A-) +c(OH-),溶液pH=7,因此得出:c(Na+)=c(A-),故C正确;
D. 在c点时溶液显碱性,因此c(OH-)>c(H+),再根据溶液电荷守恒c(Na+) +c(H+) =c(A-) +c(OH-),因此溶液中离子浓度:c(Na+)>c(A-)>c(OH-)>c(H+),故D错误。
综上所述,答案为AC。

 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
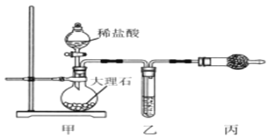
轻巧夺冠周测月考直通名校系列答案【题目】无水四氯化锡(SnCl4)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点231.9C)与Cl2 反应制备SnCl4装置如下图所示。
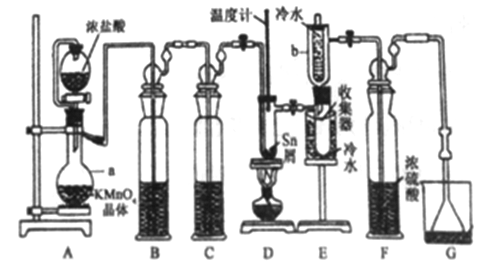
已知,① SnCl4在空气中极易水解生成SnO2xH2O;②SnCl2、SnCl4有关物理性质如下表。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
回答下列问题:
(1)仪器a的名称是__________,其中发生反应的离子方程式为________。
(2)装置B、C 中盛装的试剂分别是_______、__________。
(3)当观察到装置F液面上方出现_____现象时才开始点燃酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的有:①加快氯气与锡反应,②__________。
(4)E装置中b的作用是___________。
(5)若制得产品中含有少量Cl2,则可采用下列_____(填字母)措施加以除去。
A.加入NaOH 萃取分液 B.加入足量锡再加热蒸馏
C.加入碘化钾冷凝过滤 D.加入饱和食盐水萃取
(6)可用滴定法测定最后产品的纯度。准确称取该样品mg加入到适量浓盐酸溶解,然后再加水稀释至250 mL,用移液管移取25.00 ml,稀释后的溶液于锥形瓶中,加入两滴淀粉溶液作指示制,用cmol/L 的KIO3 标准溶液进行滴定,平行滴定3 次,平均消耗V mL的标准溶液。已知滴定时发生的反应为:Sn2++IO3-+H+→Sn4++I2+H2O(未配平)。回答下列问题:
①判断达到滴定终点的现象为____________。
②产品中SnCl2(摩尔质量为M g/mol )的含量为____%(用含m、c、V、M 的代数式表示)。
【题目】CO是生产羰基化学品的基本原料, 850℃时,在恒容密闭容器中通入CO和H2O(g),发生:CO(g)+H2O(g) ![]() H2(g)+CO2(g)
H2(g)+CO2(g) ![]() H<0,测定浓度随时间关系如下表:
H<0,测定浓度随时间关系如下表:
t/min | c(CO)/ mol·L-1 | c(H2O)/ mol·L-1 |
0 | 0.30 | 0.20 |
2 | \ | 0.10 |
3 | 0.18 | \ |
4 | \ | 0.08 |
回答下列问题
(1)t=3min时,υ(正)____________υ(逆)(选填:“>”,“<”,“=”)。
(2)0~2min,CO的平均反应速率为 ____________。
(3)上述反应中的CO平衡转化率为______;该温度下反应的平衡常数为______。
(4)850℃时,以下表中不同的起始浓度在体积可变的密闭容器中进行反应,其CO平衡转化率与原平衡相同的是______(选填a、b、c、d)。
c(CO) | c(H2O) | c(H2) | c(CO2) | |
a | 2 | 1 | 1 | 1 |
b | 0.6 | 0.4 | 0 | 0 |
c | 0.2 | 0 | 0.1 | 0.1 |
d | 1 | 1 | 1 | 1 |
(5)在一定条件下,发生下列反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示
H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示
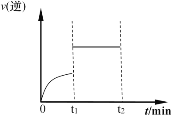
则t1时改变的某种反应条件可能是_____(填序号)。
a.增大CO浓度 b.加压
c.恒容时充入氩气 d.使用催化剂