题目内容
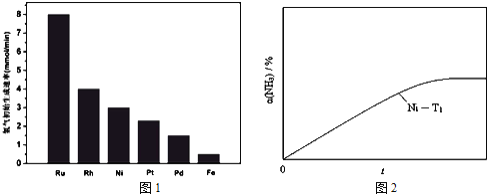
【题目】一定条件下,反应:![]() 的数据如图所示,
的数据如图所示,

下列说法正确的是( )
A.该反应的![]()
B.达平衡时,![]()
C.b点对应的平衡常数K值大于c点
D.a点对应的![]() 的平衡转化率为
的平衡转化率为![]()
【答案】D
【解析】
A. 根据图可知,随着温度的升高二氧化碳的平衡转化率下降,即升温平衡逆向移动,所以正反应为放热反应,![]() ,故A错误;
,故A错误;
B. 根据速率之比等于计量数之比可知,达平衡时,![]() ,故B错误;
,故B错误;
C. 平衡常数只与温度有关,b点温度高于c点,该反应为放热反应,升高温度平衡逆向移动,所以b点的平衡常数小于c点,故C错误;
D. a点反应物起始物质的量之比等于2,二氧化碳的平衡转化率为60%,设起始![]() 为2mol,则
为2mol,则![]() 为1mol,则二氧化碳消耗0.6mol,
为1mol,则二氧化碳消耗0.6mol,![]() 消耗1.8mol,则
消耗1.8mol,则![]() 的平衡转化率为
的平衡转化率为![]() ,故D正确;
,故D正确;
故选D。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目