��Ŀ����
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
��1����ˮ����ͨ�����ȵ�̿���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ/mol
�ٸ÷�Ӧ�ܷ��Է�������______�йأ�
����һ���¶��£���һ���ݻ�������ܱ������з���������Ӧ���������жϸ÷�Ӧ�Ѵﻯѧƽ��״̬����______��
A�������е�ѹǿ���� B��������������ܶȲ���
C��c��CO��=c��H2�� D��1 molH-H�����ѵ�ͬʱ����2mol H-O��
���ں����ܱ������м���1mol C��s����1mol H2O��g����һ���¶��³�ַ�Ӧ�ﵽƽ�⣬��������akJ����a=______131.3�����������������=����������ʼʱ�������2mol C��s����1mol H2O��g������ַ�Ӧ�ﵽƽ�⣬��������Ϊb kJ����b______a�����������������=������
��2����һ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g��
��ʵ��1�е�v��H2����ʾ�ķ�Ӧ����Ϊ______��
��830��ʱ���������г���2mol CO��10mol H2O��g������Ӧ�ﵽƽ���CO��ת����Ϊ______��
����ʵ��3Ҫ�ﵽ��ʵ��2���Ƶ�ƽ��״̬���������ʵ����������ֱ���ȣ�����t��3min����a��bӦ����Ĺ�ϵ��______���ú�a��b����ѧʽ��ʾ��
��1����ˮ����ͨ�����ȵ�̿���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ/mol
�ٸ÷�Ӧ�ܷ��Է�������______�йأ�
����һ���¶��£���һ���ݻ�������ܱ������з���������Ӧ���������жϸ÷�Ӧ�Ѵﻯѧƽ��״̬����______��
A�������е�ѹǿ���� B��������������ܶȲ���
C��c��CO��=c��H2�� D��1 molH-H�����ѵ�ͬʱ����2mol H-O��
���ں����ܱ������м���1mol C��s����1mol H2O��g����һ���¶��³�ַ�Ӧ�ﵽƽ�⣬��������akJ����a=______131.3�����������������=����������ʼʱ�������2mol C��s����1mol H2O��g������ַ�Ӧ�ﵽƽ�⣬��������Ϊb kJ����b______a�����������������=������
��2����һ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������н��з�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g��
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
| 2 | 830 | 1 | 4 | 0.8 | 0.8 | 3 |
| 3 | 830 | a | b | c | d | t |
��830��ʱ���������г���2mol CO��10mol H2O��g������Ӧ�ﵽƽ���CO��ת����Ϊ______��
����ʵ��3Ҫ�ﵽ��ʵ��2���Ƶ�ƽ��״̬���������ʵ����������ֱ���ȣ�����t��3min����a��bӦ����Ĺ�ϵ��______���ú�a��b����ѧʽ��ʾ��
��1�������Ȼ�ѧ��Ӧ����ʽ��֪����ӦΪ�������������̣�����H��0����S��0����G=��H-T��S��0��Ӧ�Է����У����Ը÷�Ӧ�Է����У����¶�Ӱ�죮
�ʴ�Ϊ���¶ȣ�
��A����Ӧǰ����������ʵ��������仯���淴Ӧ������������ʵ������ӣ�ѹǿ���������е�ѹǿ���䣬˵����Ӧ����ƽ�⣬��A��ȷ��
B���������ݻ����䣬�淴Ӧ����������������������ӣ������淴Ӧ�����ܶ�����������������ܶȲ��䣬˵����Ӧ����ƽ�⣬��B��ȷ��
C�����ݷ�Ӧ��֪����ʼ����c��CO��=c��H2��������˵����Ӧ����ƽ�⣬��C����
D��1 molH-H�����ѵ�ͬʱ����2mol H-O��������2mol H-O��ͬʱ����l molH-H����˵����Ӧ����ƽ�⣬��D��ȷ��
��ѡ��ABD��
��C��s��+H2O��g���TCO��g��+H2��g����H=+131.3kJ/mol����ʾ1molC��s����1molH2O��g����Ӧ����1molCO��g����1molH2��g�����յ�����Ϊ131.3kJ�����淴Ӧ���ڷ�Ӧ�ȣ���Ӧ�ﲻ����ȫת��������a��131.3kJ��
�������C��������ˮ���������ʵ���δ�䣬ƽ�ⲻ�ƶ�����Ӱ�췴Ӧ�ȣ���a=b��
�ʴ�Ϊ������=��
��2�����ɱ���֪5min�ڣ����������ʵ����仯��Ϊ1.6mol���������Ϊ2L������H2��ʾ�ķ�Ӧ����v��H2��=
=0.16mol/��L?min����
�ʴ�Ϊ��0.16mol/��L?min����
����ʵ��2��֪��ƽ��ʱCO2��H2�����ʵ����ֱ�Ϊ0.8mol��0.8mol��
���ڷ�Ӧ CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����1 4 0 0
�仯��mol����0.8 0.8 0.8 0.8
ƽ�⣨mol����0.2 3.2 0.8 0.8
������830��ƽ�ⳣ��k=
=
=1
��μӷ�Ӧ��CO�����ʵ���Ϊnmol����
���ڷ�Ӧ CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����2 10 0 0
�仯��mol����n n n n
ƽ�⣨mol����2-n 10-n n n
����
=1�����n=
����CO��ת����Ϊ
��100%=83.33%��
�ʴ�Ϊ��83.33%��
�۷�Ӧǰ������������䣬ʵ��2���Ƶ�ƽ��״̬���������ʵ����������ֱ���ȣ���Ϊ��Чƽ�⣬����CO��g����H2O��g�������ʵ���Ϊ1��4����a��b=1��4��b=4a�����ڵ���ƽ��ʱ��t��3min���������ʽ�ʵ��2�죬��a��1����ʹ�ô�������
�ʴ�Ϊ��b=4a��a��1����ʹ�ô�������
�ʴ�Ϊ���¶ȣ�
��A����Ӧǰ����������ʵ��������仯���淴Ӧ������������ʵ������ӣ�ѹǿ���������е�ѹǿ���䣬˵����Ӧ����ƽ�⣬��A��ȷ��
B���������ݻ����䣬�淴Ӧ����������������������ӣ������淴Ӧ�����ܶ�����������������ܶȲ��䣬˵����Ӧ����ƽ�⣬��B��ȷ��
C�����ݷ�Ӧ��֪����ʼ����c��CO��=c��H2��������˵����Ӧ����ƽ�⣬��C����
D��1 molH-H�����ѵ�ͬʱ����2mol H-O��������2mol H-O��ͬʱ����l molH-H����˵����Ӧ����ƽ�⣬��D��ȷ��
��ѡ��ABD��
��C��s��+H2O��g���TCO��g��+H2��g����H=+131.3kJ/mol����ʾ1molC��s����1molH2O��g����Ӧ����1molCO��g����1molH2��g�����յ�����Ϊ131.3kJ�����淴Ӧ���ڷ�Ӧ�ȣ���Ӧ�ﲻ����ȫת��������a��131.3kJ��
�������C��������ˮ���������ʵ���δ�䣬ƽ�ⲻ�ƶ�����Ӱ�췴Ӧ�ȣ���a=b��
�ʴ�Ϊ������=��
��2�����ɱ���֪5min�ڣ����������ʵ����仯��Ϊ1.6mol���������Ϊ2L������H2��ʾ�ķ�Ӧ����v��H2��=
| ||
| 5min |
�ʴ�Ϊ��0.16mol/��L?min����
����ʵ��2��֪��ƽ��ʱCO2��H2�����ʵ����ֱ�Ϊ0.8mol��0.8mol��
���ڷ�Ӧ CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����1 4 0 0
�仯��mol����0.8 0.8 0.8 0.8
ƽ�⣨mol����0.2 3.2 0.8 0.8
������830��ƽ�ⳣ��k=
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| 0.8��0.8 |
| 0.2��3.2 |
��μӷ�Ӧ��CO�����ʵ���Ϊnmol����
���ڷ�Ӧ CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����2 10 0 0
�仯��mol����n n n n
ƽ�⣨mol����2-n 10-n n n
����
| n��n |
| (2-n)��(10-n) |
| 5 |
| 3 |
����CO��ת����Ϊ
| ||
| 2mol |
�ʴ�Ϊ��83.33%��
�۷�Ӧǰ������������䣬ʵ��2���Ƶ�ƽ��״̬���������ʵ����������ֱ���ȣ���Ϊ��Чƽ�⣬����CO��g����H2O��g�������ʵ���Ϊ1��4����a��b=1��4��b=4a�����ڵ���ƽ��ʱ��t��3min���������ʽ�ʵ��2�죬��a��1����ʹ�ô�������
�ʴ�Ϊ��b=4a��a��1����ʹ�ô�������

��ϰ��ϵ�д�
�����Ŀ
 ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�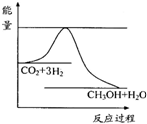 ��2009?���ݶ�ģ��ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
��2009?���ݶ�ģ��ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�