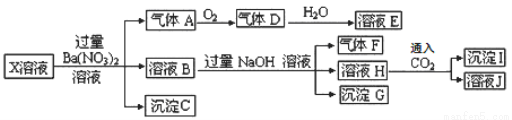
题目内容
下列各项叙述中不正确的是( )
A.10 ℃ 时NaCl溶解度为35.7g,则此时饱和NaCl 溶液的质量分数小于35.7 %
B.向Na2CO3溶液中加入少量NaHCO3 固体,溶液pH 减小
C.50mL 1.0 mol·L-1盐酸与60 mL 1.0 mol·L-1盐酸分别跟50 mL 1.1 mol·L-1NaOH溶液进行反应,中和热数值不相等
D.一定条件下,向水中加入少量NaHSO4,可使水的电离程度减小
C
【解析】
试题分析:A、根据饱和溶液的定义可知,10 ℃ 时100g水中最多溶解35.7g的氯化钠,所以所得饱和氯化钠溶液的质量分数一定小于35.7%,正确;B、碳酸根离子水解使溶液显碱性,加入少量碳酸氢钠固体,使溶液中的碳酸氢根离子浓度增大,水解平衡逆向移动,溶液碱性减弱,pH减小,正确;C、中和热与生成的水的物质的量无关,都是指强酸与强碱反应生成1mol水时放出的热量的多少,所以中和热的数值相等,错误;D、硫酸氢钠完全电离生成硫酸根离子、氢离子、钠离子,而氢离子浓度增大,对水的电离起抑制作用,所以水的电离程度减小,正确,答案选C。
考点:考查溶液质量分数的判断,离子平衡的判断,中和热的判断

根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO | Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO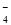 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
(10分)某种溶液仅含下表离子中的5种(不考虑水的电离与离子水解),且各种离子的物质的量均为1 mol。
阳离子 | K+ Ba2+ Fe2+ Al3+ Fe3+ Mg2+ |
阴离子 | OH- HCO3- CO32- Cl- NO3- SO42- |
若向原溶液中加入足量的盐酸,有无色气体生成。经分析反应后溶液中阴离子的种类没有变化。
(1)溶液中______(填“一定”、“一定不”或“可能”)含有HCO3-或CO32-,理由是________________。
(2)原溶液中所含的阴离子为__________,阳离子为__________。
(3)向原溶液中加入足量的盐酸,有无色气体生成的离子反应方程式为__________________。
(4)若向原溶液中加入足量的氢氧化钠溶液,充分反应后将沉淀过滤、洗涤、干燥灼烧至恒重,得到固体质量为__________g。
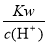 =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42-
=10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42-