题目内容
6.根据下列叙述,写出元素(1--18号)名称并画出原子结构示意图.(1)某元素原子核外M层电子数是L层电子数的一半硅、

(2)某元素原子的最外层电子数是次外层电子数的1.5倍硼、

(3)某元素的单质在常温下最易和O2反应产生白色固体钠、

(4)某元素的次外层电子数是最外层电子数的一半碳、
 .
.
分析 (1)元素原子核外M层电子数是L层电子数的一半,M层电子数为4,则为Si;
(2)元素原子的最外层电子数是次外层电子数的1.5倍,原子只能有2个电子层,最外层电子数为3,故为硼元素;
(3)元素的单质在常温下最易和O2反应产生白色固体,则为钠元素;
(4)元素的次外层电子数是最外层电子数的一半,原子只能有2个电子层,最外层电子数为4,故为C.
解答 解:(1)元素原子核外M层电子数是L层电子数的一半,M层电子数为4,则为Si,原子结构示意图为: ,故答案为:硅;
,故答案为:硅; ;
;
(2)元素原子的最外层电子数是次外层电子数的1.5倍,原子只能有2个电子层,最外层电子数为3,故为硼元素,原子结构示意图为: ,
,
故答案为:硼; ;
;
(3)元素的单质单质在常温下最易和O2反应产生白色固体,则为钠元素,原子结构示意图为: ,故答案为:钠;
,故答案为:钠; ;
;
(4)元素次外层电子数是最外层电子数的一半,原子只能有2个电子层,最外层电子数为4,故为C,原子结构示意图为: ,
,
故答案为:碳; .
.
点评 本题考查核外电子排布,比较基础,推断元素是关键,注意理解掌握原子结构示意图的书写.

练习册系列答案
相关题目
16.下列四个数据是在不同条件下测出的合成氨反应N2+3H2?2NH3的速率,其中最快是( )
| A. | V(H2)═0.3 mol/(L•min) | B. | V(N2)═0.1mol/(L•min) | ||
| C. | V(NH3)═0.15mol/(L•min) | D. | V(N2)═0.2mol/(L•min) |
17.将64g铜与一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为33.6L.欲使反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要40%的双氧水的质量为( )
| A. | 85g | B. | 79g | C. | 116g | D. | 58g |
1.向AgNO3溶液中加入一定质量Fe和Al的混合溶液,充分反应后过滤,得到滤渣和浅绿色滤液.下列说法正确的是( )
| A. | 滤液中一定含有Al3+、Ag+ | B. | 滤液中一定含有Fe2+、Ag+ | ||
| C. | 滤渣中一定含有Fe | D. | 滤渣中一定含有Ag |
11.下列有水参加的反应,其中是氧化还原反应且水既不是氧化剂又不是还原剂的是( )
| A. | 钠跟水 | B. | 氧化钠跟水 | C. | 过氧化钠跟水 | D. | 电解水 |
18.下列说法正确的是( )
| A. | 由不同种类的原子构成的物质不可能是单质 | |
| B. | 葡萄糖注射液不能产生丁达尔现象,不属于胶体 | |
| C. | 蔗糖、硫酸钡和氨气分别属于非电解质、强电解质和弱电解质 | |
| D. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
15. 用以下几种常见有机物填写下列空白:
用以下几种常见有机物填写下列空白:
a.CH4 b.C2H4 c.C6H6 d.C2H5OH e.CH3COOH
(1)等质量的CH4、C2H4、C6H6三种烃完全燃烧消耗O2的量由多到少的顺序是a>b>c(用序号表示).
(2)等物质的量混合的甲烷和乙酸蒸气完全燃烧所得二氧化碳和水蒸气的物质的量之比为3:4.
(3)由乙烯和乙醇蒸气组成的混合气体1mol完全燃烧所需氧气在标准状况下的体积为67.2L.
(4)由两种气态烃组成的混合气体完全燃烧后,将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收).
根据实验数据填空:
①假设广口瓶里生成一种正盐,其质量为15g.
②混合气体中C、H两元素的物质的量之比为3:8.
③若混合气体是由CH4和C2H4组成,则二者的体积比为1:1.
 用以下几种常见有机物填写下列空白:
用以下几种常见有机物填写下列空白:a.CH4 b.C2H4 c.C6H6 d.C2H5OH e.CH3COOH
(1)等质量的CH4、C2H4、C6H6三种烃完全燃烧消耗O2的量由多到少的顺序是a>b>c(用序号表示).
(2)等物质的量混合的甲烷和乙酸蒸气完全燃烧所得二氧化碳和水蒸气的物质的量之比为3:4.
(3)由乙烯和乙醇蒸气组成的混合气体1mol完全燃烧所需氧气在标准状况下的体积为67.2L.
(4)由两种气态烃组成的混合气体完全燃烧后,将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收).
| 实验前 | 实验后 | |
| (干燥剂+U形管)的质量 | 101.1g | 104.7g |
| (澄清石灰水+广口瓶)的质量 | 312.0g | 318.6g |
①假设广口瓶里生成一种正盐,其质量为15g.
②混合气体中C、H两元素的物质的量之比为3:8.
③若混合气体是由CH4和C2H4组成,则二者的体积比为1:1.
 人们对苯的认识有一个不断深化的过程.
人们对苯的认识有一个不断深化的过程.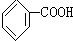 和生石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式:
和生石灰的混合物得到液体,命名为苯,写出苯甲酸钠与碱石灰共热生成苯的化学方程式: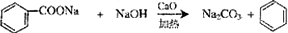 (NaOH参与反应)
(NaOH参与反应)
 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填“稳定”或“不稳定”).