题目内容
下列方法不能证明氢氟酸(HF)是弱电解质的是( )
| A、分别测定比较相同浓度氢氟酸和盐酸的pH值 |
| B、比较相同浓度氢氟酸和盐酸的导电能力 |
| C、用大小形状相同的镁条分别与相同浓度氢氟酸和盐酸反应,比较反应速率的快慢 |
| D、取相同体积相同浓度的氢氟酸和盐酸分别与NaOH溶液反应,比较消耗NaOH溶液的体积 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A.氯化氢是强电解质,完全电离,相同浓度氢氟酸和盐酸的pH值如果相同可以说明氟化氢能完全电离;
B.电解质溶液的导电能力与自由离子的浓度成正比;
C.镁条与酸反应产生氢气快慢,与溶液中氢离子浓度有关;
D.氟化氢和氯化氢都是一元酸,中和氢氧化钠的能力相同.
B.电解质溶液的导电能力与自由离子的浓度成正比;
C.镁条与酸反应产生氢气快慢,与溶液中氢离子浓度有关;
D.氟化氢和氯化氢都是一元酸,中和氢氧化钠的能力相同.
解答:
解:A.氯化氢是强电解质,完全电离,相同浓度氢氟酸和盐酸的pH值如果相同可以说明氟化氢能完全电离,故A正确;
B.氟化氢和氯化氢都是一元酸,盐酸是强酸,如果相同浓度的两种酸导电能力相同,可以证明氢氟酸是强酸,否则,为弱酸,故B正确;
C.镁条与酸反应产生氢气快慢,与溶液中氢离子浓度有关,相同浓度氢氟酸和盐酸反应,如果产生氢气的速率相同,说明氢氟酸是强酸,否则,为弱酸,故C正确;
D.氟化氢和氯化氢都是一元酸,中和氢氧化钠的能力相同,故D错误;
故选:D.
B.氟化氢和氯化氢都是一元酸,盐酸是强酸,如果相同浓度的两种酸导电能力相同,可以证明氢氟酸是强酸,否则,为弱酸,故B正确;
C.镁条与酸反应产生氢气快慢,与溶液中氢离子浓度有关,相同浓度氢氟酸和盐酸反应,如果产生氢气的速率相同,说明氢氟酸是强酸,否则,为弱酸,故C正确;
D.氟化氢和氯化氢都是一元酸,中和氢氧化钠的能力相同,故D错误;
故选:D.
点评:本题考查了弱酸判断的方法,题目难度不大,把握弱电解质不能完全电离的特点是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明反应A(s)+2B(g)?C(g)+D(g) 已达到平衡状态的是( )
①混合气体的压强,②混合气体的密度,③B的物质的量浓度,④气体的总物质的量,⑤混合气体的平均相对分子质量,⑥V正(B)=2V逆.
①混合气体的压强,②混合气体的密度,③B的物质的量浓度,④气体的总物质的量,⑤混合气体的平均相对分子质量,⑥V正(B)=2V逆.
| A、①②③ | B、②③④⑥ |
| C、②③⑤⑥ | D、①③④⑤ |
已知某元素的阴离子Rn-,其原子核内的中子数为A-x+n,其中A为质量数.则W g Rn-中的电子总数为(NA为阿伏加德罗常数)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
如图中的三种常用金属的开发利用之所以有先后,主要取决于( )

| A、金属的导电性强弱 |
| B、金属在地壳中的含量多少 |
| C、金属的化合价高低 |
| D、金属的活动性大小 |
下列物质中只含有离子键的是( )
| A、Na2O2 |
| B、CaCl2 |
| C、NO2 |
| D、KNO3 |
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是( )
| A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量少 |
| B、盐酸和醋酸都可用相应的钠盐和浓硫酸反应制取 |
| C、相同pH的等体积盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大 |
| D、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
下列离子方程式正确的是( )
| A、向氢氧化钡溶液中加硫酸溶液 Ba2++SO42-═BaSO4↓ |
| B、用食醋与苏打溶液反应(主要成分是碳酸钠)2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O |
| C、石灰乳与碳酸钠溶液混合Ca2++CO32-═CaCO3↓ |
| D、氧化铁溶于稀硝酸 Fe2O3+6H+═2Fe3++3H2O |
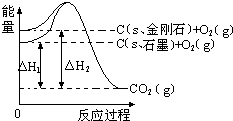 如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法不正确的是( )
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法不正确的是( )| A、C(s、金刚石)C═(s、石墨)△H=-1.9 kJ?mol-1 |
| B、石墨和金刚石的转化是化学变化 |
| C、1mol金刚石完全燃烧放出的能量比1mol石墨完全燃烧放出的能量多 |
| D、金刚石的稳定性强于石墨 |
设NA是阿伏伽德罗常数的数值.下列说法正确的是( )
| A、1L 0.1mol/L的醋酸溶液中,CH3COO-的数目为0.1NA |
| B、标准状况下,8gSO3中含有氧原子的数目为0.3NA |
| C、7.8gNa2O2中含有的阳离子数目为0.1NA |
| D、6mol的二氧化氮和足量的水反应生成硝酸,转移8NA个的电子 |