题目内容
【题目】
I.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:
2Mg5Al3(OH)19(H2O)4![]() 27H2O↑+10MgO+3A12O3
27H2O↑+10MgO+3A12O3
(1)写出该化合物作阻燃剂的两条依据____________________________________。
(2)用离子方程式表示除去固体产物中A12O3的原理________________________。
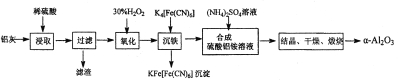
II.以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为A12O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
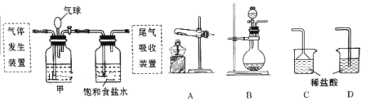
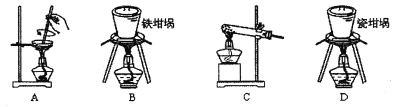
(1)用图中“滤渣”和NaOH焙烧制备硅酸钠,可采用的装置为_______(填选项编号)。
(2)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为____________________。
(3)若用调节溶液的pH“沉铁”,则得到Fe(OH)3,己知:
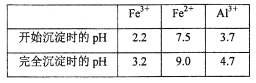
为保证产品的纯度,最好选用下列物质中的_______调节pH(填字母),调节pH的范围为_____。
a.A12O3
B.H2SO4
C.NaOH
D.Na2CO3
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
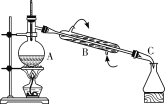
将产生的气体通过下图所示的装置。
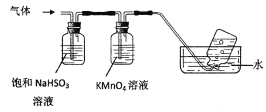
①集气瓶中收集到的气体是_____________________(填化学式)。
②KMnO4溶液褪色,发生的离子反应方程式为_________________________________。
【答案】
Ⅰ.(1)反应吸热降低温度,固体氧化物隔绝空气,水蒸气稀释空气
(2)Al2O3+2OH-=2AlO2-+H2O
Ⅱ.(1)B
(2)静置,溶液澄清后,继续向上层清液中滴加K4[Fe(CN)6]溶液,若无现象,则溶液中不含有铁离子,反之,则有。(其它合理答案)
(3)a3.2≤pH<3.7
(4)①N2②2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+
【解析】
试题分析:Ⅰ.(1)2Mg5Al3(OH)19(H2O)4![]() 27H2O↑+10MgO+3Al2O3,分解反应是吸热反应,降低温度,生成的氧化镁和氧化铝都是熔点很高的氧化物,附着表面会阻止燃烧,水蒸气稀释空气;
27H2O↑+10MgO+3Al2O3,分解反应是吸热反应,降低温度,生成的氧化镁和氧化铝都是熔点很高的氧化物,附着表面会阻止燃烧,水蒸气稀释空气;
(2)氧化镁是碱性氧化物溶于酸,氧化铝是两性氧化物溶于酸、碱溶于,加入氢氧化钠溶于溶解后过滤除去,反应的离子方程式为:Al2O3+2OH-=2AlO2-+H2O;
Ⅱ.(1)能够焙烧固体的装置是坩埚,NaOH能和二氧化硅反应生成硅酸钠,所以不能采用瓷坩埚灼烧,所以应该采用铁坩埚,故选B;
(2)铁离子和铁氰化钾反应产生沉淀,其检验方法是:静置,溶液澄清后,继续向上层清液中滴加K4[Fe(CN)6]溶液,若无现象,则溶液中不含有铁元素,反之,则有;
(3)结合除杂原则,不引入新的杂质,只能选用Al2O3即选项a来调节溶液pH;调节pH的目的是使Fe3+完全沉淀,而Al3+不沉淀,即溶液的pH范围为3.2≤pH<3.7;
(4)①煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)212H2O]═2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,混合气体通入饱和的亚硫酸氢钠溶液中,氨气和三氧化硫溶解,剩余气体通入高锰酸钾溶液,二氧化硫被氧化生成硫酸根离子,剩余的气体N2采用排水法收集;
②二氧化硫被酸性高锰酸钾溶液氧化而导致KMnO4溶液褪色,二者发生氧化还原反应生成锰离子、硫酸根离子和氢离子,离子方程式为2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+。

 每课必练系列答案
每课必练系列答案