题目内容
下列叙述中,能证明某物质是强电解质或弱电解质的是( )
| A、某物质熔化时不导电,则该物质为弱电解质 |
| B、某物质不是离子化合物,而是极性共价化合物,则该物质为弱电解质 |
| C、某一元酸2 mol与足量Zn完全反应生成1 molH2,则该酸为强酸 |
| D、溶液中已电离的离子和未电离的分子共存,则该物质为弱电解质 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐,以此解答.
解答:
解:A.熔化时不导电,说明没有自由移动的离子,但不是弱电解质的特征,如蔗糖是非电解质,HCl为强电解质,熔化时不导电,故A错误;
B.电解质的强弱是根据其电离程度划分的,与是离子化合物还是共价化合物无关,如HCl为极性化合物,但为强电解质,故B错误;
C.无论强酸还是弱酸,如完全反应,则一元酸2 mol与足量Zn完全反应生成1 molH2,故C错误;
D.溶液中溶质电离出的离子与未电离的分子共同存在,说明该溶质只有部分电离,所以为弱电解质,故D正确.
故选D.
B.电解质的强弱是根据其电离程度划分的,与是离子化合物还是共价化合物无关,如HCl为极性化合物,但为强电解质,故B错误;
C.无论强酸还是弱酸,如完全反应,则一元酸2 mol与足量Zn完全反应生成1 molH2,故C错误;
D.溶液中溶质电离出的离子与未电离的分子共同存在,说明该溶质只有部分电离,所以为弱电解质,故D正确.
故选D.
点评:本题考查了弱电解质的判断,根据电解质的电离程度来判断,易错选项是C,注意电解质的强弱与溶液导电能力无关,强电解质溶液的导电能力不一定强,导电能力强的溶液不一定是强电解质溶液,为易错点.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 |
| B、酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
| C、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| D、由单质A转化为单质B,△H=+119KJ/mol,可知单质A比单质B稳定 |
下列实验基本操作(或实验注意事项)中,主要是出于实验安全考虑的是( )
| A、可燃性气体的验纯 |
| B、过滤时玻璃棒不能在漏斗内搅拌 |
| C、使用分液漏斗前要检验是否漏液 |
| D、滴管不能交叉使用 |
 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量.则下列说法正确的是( )
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量.则下列说法正确的是( )| A、N4属于一种新型的化合物 |
| B、1mo1N4气体转变为N2将放出882kJ热量 |
| C、N4与N2互为同分异构体 |
| D、N4沸点比P4(白磷)沸点高 |
肯定不会影响化学平衡的因素是( )
| A、温度 | B、浓度 | C、压强 | D、催化剂 |
下列叙述中错误的是( )
| A、钠在空气中燃烧生成氧化钠 |
| B、钠是强还原剂 |
| C、钠在空气中燃烧生成过氧化钠 |
| D、钠燃烧发出黄色火焰 |
下列各对物质中,不是互为同系物的是( )
A、环己烷与  |
B、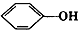 和 和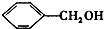 |
| C、甲苯和二甲苯 |
| D、乙酸和硬脂酸 |
镁带在空气中燃烧生成的固体产物主要是氧化镁和氮化镁.将燃烧后的固体产物溶解在60mL浓度为2.0mol/L的盐酸中,(氮化镁和盐酸反应的化学方程式为:Mg3N2+8HCl═3MgCl2+2NH4Cl)以20mL 0.5mol/L的氢氧化钠溶液中和多余的盐酸,然后在此溶液中加入过量的碱,把氨全部蒸发出来,用稀盐酸吸收,稀盐酸增重0.17g.镁带的质量为( )
| A、0.6 g |
| B、1.2 g |
| C、2.4 g |
| D、3.6 g |
下列说法正确的是( )
| A、形成离子键的阴阳离子间只存在静电吸引力 |
| B、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C、元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
| D、原子及其离子的核外电子层数等于该元素所在的周期数 |