题目内容
A、B、C、D都是短周期元素,原子半径:D>C>A>B.已知A、B同周期,A、C同主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的3倍.下列说法中正确的是
( )
( )
分析:根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: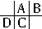 ,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,根据元素对应原子的结构判断元素在周期表中的位置,结合元素对应化合物的性质解答该题.
,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,根据元素对应原子的结构判断元素在周期表中的位置,结合元素对应化合物的性质解答该题.
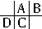 ,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,根据元素对应原子的结构判断元素在周期表中的位置,结合元素对应化合物的性质解答该题.
,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,根据元素对应原子的结构判断元素在周期表中的位置,结合元素对应化合物的性质解答该题.解答:解:根据原子半径D>C>A>B,且A、B同周期,A、C同主族,推知A、B、C、D在周期表中的大致相对位置为: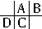 ,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,
,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,
A.由以上分析可知A、C两元素处在元素周期表中的第ⅢA族,故A错误;
B.B、D两元素可形成两种离子化合物,分别为Na2O、Na2O2,其阴、阳离子数之比均为1:2,故B正确;
C.B、C、D三种元素组成的化合物的化学式为NaAlO2,故C错误;
D.B、C、D三种元素的简单离子的核外电子排布相同,核电荷数越大,离子半径越小,应为B>D>C,故D错误.
故选B.
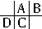 ,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,
,C的原子核内的质子数等于A、B原子核内的质子数之和,可知原子序数C=A+8,故B为8号元素氧.因A、C为主族元素,且C最外层电子数为D的3倍,故D为Na元素,C为Al元素,A为B元素,A.由以上分析可知A、C两元素处在元素周期表中的第ⅢA族,故A错误;
B.B、D两元素可形成两种离子化合物,分别为Na2O、Na2O2,其阴、阳离子数之比均为1:2,故B正确;
C.B、C、D三种元素组成的化合物的化学式为NaAlO2,故C错误;
D.B、C、D三种元素的简单离子的核外电子排布相同,核电荷数越大,离子半径越小,应为B>D>C,故D错误.
故选B.
点评:本题考查原子结构与元素周期律的关系,题目难度较大,注意根据元素在周期表中的位置关系以及原子结构特点证明推断元素种类为解答该题的关键,注意元素周期律的递变规律的判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

