题目内容
12.消防安全与化学科学密切相关,下列有关举措合理的是( )| A. | KNO3、KClO3与单质S、C2H5OH混搭存放在同一库房间 | |
| B. | 金属钠、二硅化钙着火时,直接用高压水枪喷水扑灭 | |
| C. | 燃气中添加具有明显臭味的四氢噻吩杂质,用以警示气体的泄漏 | |
| D. | 剧毒的NaCN溶液泄漏时,直接将其冲入下水道,让其自然消解 |
分析 A.KNO3、KClO3有氧化性;
B.钠能与水反应生成氢气;
C.四氢噻吩有臭味;
D.剧毒的NaCN溶液会污染下水道中的水.
解答 解:A.KNO3、KClO3有氧化性,单质S、C2H5OH易燃烧,放在一起可能发生爆炸,故A错误;
B.钠能与水反应生成氢气,氢气易爆炸,故B错误;
C.四氢噻吩有臭味,能起警示作用,故C正确;
D.剧毒的NaCN溶液会污染下水道中的水,造成环境污染,故D错误.
故选C.
点评 本题考查化学实验室安全及事故处理,该题是基础性试题的考查,难度不大,侧重对学生实验基础知识的检验和训练,有利于培养学生的实验能力.在实验过程中应学会处理常见意外事故的方法技巧.

练习册系列答案
相关题目
16.某羧酸酯的分子式为C19H28O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
| A. | C15H24O5 | B. | C15H18O4 | C. | C15H20O5 | D. | C15H12O5 |
20.某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)氨基甲酸铵(NH2COONH4)分解反应是NH2COONH4(s)?2NH3(g)+CO2(g).
①某物质的标准摩尔生成焓是指在标准状态下由稳定单质生成1mol该物质时的反应焓变.
例如:CH3COOH的标准摩尔生成焓是指如下反应在标准状态下的焓变△H(CH3COOH)C(s)+O2(g)+H2(g)═CH3COOH(l)△H(CH3COOH)
已知NH2COONH4(s)、NH3(g)和CO2(g)的标准摩尔生成焓分别为△H1、△H2和△H3,则上述NH2COONH4分解反应的反应热△H=2△H2+△H3-△H1
②将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
实验测得不同温度下的平衡数据列于下表:
i.可以判断该分解反应已经达到化学平衡的是BC.
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
ii.根据表中数据,列式计算25.0℃时的分解平衡常数:1.6×10-8.(保留两位有效数字)
iii.取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.下列说法正确的是c.
a、恒温、压缩容器体积,再次达到平衡后,容器内的压强大于原平衡压强
b、恒温、增大容器体积,再次达到平衡后,容器内的c(CO2)小于原平衡时的浓度
c、固定活塞、升高温度,再次达到平衡后,容器内的压强大于原平衡时的压强.
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.
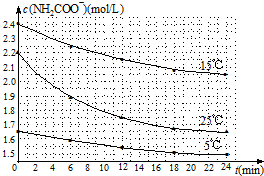
①计算25℃时,0~6min氨基甲酸铵水解反应的平均速率0.05mol/(L•min).
②根据图中信息,如何说明水解反应速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
(1)氨基甲酸铵(NH2COONH4)分解反应是NH2COONH4(s)?2NH3(g)+CO2(g).
①某物质的标准摩尔生成焓是指在标准状态下由稳定单质生成1mol该物质时的反应焓变.
例如:CH3COOH的标准摩尔生成焓是指如下反应在标准状态下的焓变△H(CH3COOH)C(s)+O2(g)+H2(g)═CH3COOH(l)△H(CH3COOH)
已知NH2COONH4(s)、NH3(g)和CO2(g)的标准摩尔生成焓分别为△H1、△H2和△H3,则上述NH2COONH4分解反应的反应热△H=2△H2+△H3-△H1
②将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
ii.根据表中数据,列式计算25.0℃时的分解平衡常数:1.6×10-8.(保留两位有效数字)
iii.取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.下列说法正确的是c.
a、恒温、压缩容器体积,再次达到平衡后,容器内的压强大于原平衡压强
b、恒温、增大容器体积,再次达到平衡后,容器内的c(CO2)小于原平衡时的浓度
c、固定活塞、升高温度,再次达到平衡后,容器内的压强大于原平衡时的压强.
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.

①计算25℃时,0~6min氨基甲酸铵水解反应的平均速率0.05mol/(L•min).
②根据图中信息,如何说明水解反应速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
7.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LCH4中含有氢原子数目为4NA | |
| B. | 1molNa2O2中含有的阴离子和阳离子的数目为2NA | |
| C. | 0.1mol/LCu(NO3)2溶液中含有的NO3-数目为0.2NA | |
| D. | 28gN2中所含的原子数目为NA |
17.下列指定反应的离子方程式错误的是( )
| A. | NO2溶于水:3NO2+H2O=2H++2NO3-+NO | |
| B. | 用惰性电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu↓+4H++O2↑ | |
| C. | NaClO溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3- | |
| D. | NaAlO2溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
4.下列有机物分子中,所有的碳原子可能不处于同一平面上的是( )
| A. | CH2=CH-CH3 | B. | C6H5-CH=CH2 | C. | C6H5-CH3 | D. | CH2=CH2 |
1.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数为0.2NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
2.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为20.则下列说法不正确的是( )
| X | Y | |||
| W | Z |
| A. | 最高价氧化物的水化物的酸性:X<Z | |
| B. | 原子半径大小:Y<W | |
| C. | X的非金属性大于Y | |
| D. | W的最高价氧化物的水化物具有两性 |
