题目内容
1.化合物A是合成天然橡胶的单体,其分子式为C5H8.A的同分异构体中不含聚集双烯(C=C=C)结构单元的链状烃还有6种,写出其中互为立体异构体的(顺反异构)化合物的结构简式 .
.
分析 化合物A是合成天然橡胶的单体,为异戊二烯,其分子式为C5H8.结构简式为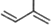 ,双键碳上连接不同的原子或原子团,存在顺反异构,链烃中二烯和炔烃为同分异构体,据此书写同分异构体和结构简式.
,双键碳上连接不同的原子或原子团,存在顺反异构,链烃中二烯和炔烃为同分异构体,据此书写同分异构体和结构简式.
解答 解:化合物A是合成天然橡胶的单体,为异戊二烯,其分子式为C5H8.结构简式为 ,双键碳上连接不同的原子或原子团,存在顺反异构,链烃中二烯和炔烃为同分异构体,同分异构体结构简式为:
,双键碳上连接不同的原子或原子团,存在顺反异构,链烃中二烯和炔烃为同分异构体,同分异构体结构简式为: ,除去其本身,所以还有6种,互为立体异构体的化合物为
,除去其本身,所以还有6种,互为立体异构体的化合物为 ,
,
故答案为:6; .
.
点评 本题考查有机物的推断,注意书写同分异构体时应按照顺序书写,如按照碳链异构、官能团位置异构、类别异构(如同碳数的二烯烃与炔烃,醇与醚,羧酸与酯、羟基醛等属于类别异构)和顺反异构等,受思维定势影响,只考虑二烯烃而不去考虑炔烃,则就只能得到3种同分异构体,从而错答同分异构体的种数,为易错点,题目难度中等.

练习册系列答案
相关题目
11.下列有机物能使酸性KMnO4溶液褪色的是( )
①CH3CH2CH3 ② ③CH3CH2CH2Br
③CH3CH2CH2Br
④CH3CH2CH2OH ⑤CH3CH2CHO ⑥HCOOCH2CH3.
①CH3CH2CH3 ②
 ③CH3CH2CH2Br
③CH3CH2CH2Br④CH3CH2CH2OH ⑤CH3CH2CHO ⑥HCOOCH2CH3.
| A. | ①③⑤ | B. | ②④⑥ | C. | ②③④ | D. | ④⑤⑥ |
12.下列叙述错误的是( )
| A. | 与  互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 | |
| B. | 含有5个碳原子的某饱和链烃,其一氯取代物的结构可能有3种 | |
| C. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,得到的结构可能有6种 | |
| D. | 菲的结构简式为 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
9.烯烃在一定条件下发生氧化反应时,碳碳双键发生断裂,RCH═CHR1可以氧化成RCHO和R1CHO.在该条件下,下列烯烃分别被氧化后,产物中可能有乙醛的是( )
| A. | CH3CH2CH=CHCH2CH3 | B. | CH2=CHCH2CH2CH3 | ||
| C. | CH3CH=CHCH2CH2CH3 | D. | CH3CH2CH=C(CH3)2 |
16.在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H<0.下列各项能说明该反应已经达到平衡状态的是 ( )
| A. | 容器内气体密度保持不变 | |
| B. | 容器内温度不再变化 | |
| C. | 断裂1mol N≡N键的同时,生成6mol N-H键 | |
| D. | 反应消耗N2、H2与产生NH3的速率之比1:3:2. |
6.H2S在金属离子的鉴定分析、煤化工等领域都有重要应用.请回答:
Ⅰ、工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时生成两种能参与大气循环的氧化物.
(1)该反应的化学方程式为4SO2+3CH4═4H2S+3CO2+2H2O.
II.H2S可用于检测和沉淀金属阳离子.
(2)H2S的第一步电离方程式为H2S?H++HS-.
(3)己知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27,该温度下,向浓度均为0.1mol•L-1的CdCl2和SnCl2的混合溶液中通人H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=8.0×10-3mol/L(溶液体积变化忽略不计).
Ⅲ.H2S是煤化工原料气脱硫过程的重要中间体.反应原理为:
ⅰ.COS(g)+H2(g)?H2S(g)+CO(g)△H=+7kJ•mol-1;
ⅱ.CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42kJ•mol-1;
(4)己知:断裂1mol分子中的化学键所需吸收的能量如下表所示.
表中x=1076.
(5)向10L容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),进行上述两个反应.其他条件不变时,体系内CO的平衡体积分数与温度(T)的关系如图所示.

①随着温度升高,CO的平衡体积分数增大(填“增大”或“减小”),原因为反应I为吸热反应,升高温度,平衡正向移动,CO的平衡体积分数增大;反应II为放热反应,升高温度,平衡逆向移动,CO的平衡体积分数也增大.
②T1℃时,测得平衡时体系中COS的物质的童为0.80mol.则该温度下,COS的平衡转化率为20%;反应i的平衡常数为0.044(保留两位有效数字).
Ⅰ、工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时生成两种能参与大气循环的氧化物.
(1)该反应的化学方程式为4SO2+3CH4═4H2S+3CO2+2H2O.
II.H2S可用于检测和沉淀金属阳离子.
(2)H2S的第一步电离方程式为H2S?H++HS-.
(3)己知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27,该温度下,向浓度均为0.1mol•L-1的CdCl2和SnCl2的混合溶液中通人H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=8.0×10-3mol/L(溶液体积变化忽略不计).
Ⅲ.H2S是煤化工原料气脱硫过程的重要中间体.反应原理为:
ⅰ.COS(g)+H2(g)?H2S(g)+CO(g)△H=+7kJ•mol-1;
ⅱ.CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42kJ•mol-1;
(4)己知:断裂1mol分子中的化学键所需吸收的能量如下表所示.
| 分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
| 能量/kJ•mol-1 | 1319 | 442 | x | 678 | -930 | 1606 |
(5)向10L容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),进行上述两个反应.其他条件不变时,体系内CO的平衡体积分数与温度(T)的关系如图所示.

①随着温度升高,CO的平衡体积分数增大(填“增大”或“减小”),原因为反应I为吸热反应,升高温度,平衡正向移动,CO的平衡体积分数增大;反应II为放热反应,升高温度,平衡逆向移动,CO的平衡体积分数也增大.
②T1℃时,测得平衡时体系中COS的物质的童为0.80mol.则该温度下,COS的平衡转化率为20%;反应i的平衡常数为0.044(保留两位有效数字).
13. 的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)( )
的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)( )
 的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)( )
的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
10.除第一周期外,关于同周期主族元素的下列变化规律的叙述中不正确的是( )
| A. | 从左到右,原子半径逐渐减小 | |
| B. | 从左到右,元素原子的得电子能力减弱,失电子能力增强 | |
| C. | 从左到右,气态氢化物的稳定性增强 | |
| D. | 从左到右,元素最高价氧化物对应水化物碱性减弱,酸性增强 |
 合理应用和处理氮的化合物,在生产生活中有重要意义.
合理应用和处理氮的化合物,在生产生活中有重要意义.