题目内容
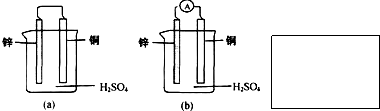
将锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池(如图所示).下列叙述不正确的是( )
A.铜片质量不变
B.锌片发生氧化反应
C.该装置将化学能转变为电能
D.电流从锌片流向铜片
【答案】分析:A、原电池的正极金属不参与化学反应,质量不变;
B、原电池的负极发生的是失电子的氧化反应;
C、原电池是将化学能转化为电能的装置;
D、原电池中,电流流向和电子流向相反,从正极流向负极.
解答:解:A、锌片和铜片用导线相连后插入稀硫酸溶液中构成的原电池中,金属铜做正极,该极产生氢气,所以电极质量不变,故A正确;
B、锌片和铜片用导线相连后插入稀硫酸溶液中构成的原电池中,金属锌做负极,发生氧化反应,故B正确;
C、该装置是原电池装置,将化学能转化为电能,故C正确;
D、原电池中,电流流向和电子流向相反,应从正极流向负极,即从铜片流向锌片,故D错误.
故选D.
点评:本题考查学生原电池的工作原理,可以根据所学知识进行回答 难度不大.
B、原电池的负极发生的是失电子的氧化反应;
C、原电池是将化学能转化为电能的装置;
D、原电池中,电流流向和电子流向相反,从正极流向负极.
解答:解:A、锌片和铜片用导线相连后插入稀硫酸溶液中构成的原电池中,金属铜做正极,该极产生氢气,所以电极质量不变,故A正确;
B、锌片和铜片用导线相连后插入稀硫酸溶液中构成的原电池中,金属锌做负极,发生氧化反应,故B正确;
C、该装置是原电池装置,将化学能转化为电能,故C正确;
D、原电池中,电流流向和电子流向相反,应从正极流向负极,即从铜片流向锌片,故D错误.
故选D.
点评:本题考查学生原电池的工作原理,可以根据所学知识进行回答 难度不大.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目