��Ŀ����
10�� ����Fe�������Ͳ��ϣ����г�ǿ���ԡ���Ч���ԣ�ij��ѧС��̽����������̼��������ȡ�������ۣ���ʵ�������ͼ�����ȡ�֧��װ��ʡ�ԣ�
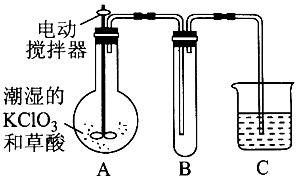
����Fe�������Ͳ��ϣ����г�ǿ���ԡ���Ч���ԣ�ij��ѧС��̽����������̼��������ȡ�������ۣ���ʵ�������ͼ�����ȡ�֧��װ��ʡ�ԣ���1��a��������������ƿ��Ũ��������������������е�ˮ�������������������
��2����Һ©��������һ��ʱ����ٶ�Cװ�ü��ȣ�����������Ŀ�����ų���ϵ�ڵĿ�������ֹ����ʵ�飬��ֹ��ը����Ӧһ��ʱ���D�б�����E����Һ����ǣ�C�з�����Ӧ�Ļ�ѧ����ʽΪFeCO3+H2$\frac{\underline{\;\;��\;\;}}{\;}$Fe+CO2+H2O��
��3����Ӧ�����۲쵽Bװ�������ݲ������죬��Ӧ���еIJ����ǵ���A�з�Һ©����������������μ��ٶȣ�
��4����Ӧһ��ʱ���B�в�������̫�����ٵμ����ᷴӦ�������мӿ쵫�����ԣ����������м���������ͭ�ٵ�����Zn��Ӧ����Ӧ�������Լӿ죬ԭ����п������ͭ��Ӧ����ͭ��ͭ��п�γ�ԭ��أ�пΪ���������ӿ��˷�Ӧ���ʣ�
��5������̼�������к�����Ԫ�ص�ʵ�鷽����ȡ����FeCO3������������ȫ�ܽ⣬�ټ�������K3[Fe��CN��3]��Һ��������ɫ��������̼�������к�����Ԫ�أ�
���� ��������̼��������ȡ�������ۣ���ʵ��װ�ÿ�֪��A�з���Zn+H2SO4=ZnSO4+H2����B��Ũ�������������C�з���FeCO3+H2 $\frac{\underline{\;\;��\;\;}}{\;}$Fe+CO2+H2O��D����ˮ����ͭ������E��ʯ��ˮ����ǣ���˵��C����Ӧ�ķ�������ʵ������������ʱ���ȷ�����ը��Ӧ���Ʊ���������װ���еĿ����ų��������������ټ���C�������ԭ��ؿɼӿ췴Ӧ���ʡ�����������K3[Fe��CN��3]���������ɫ���������
��� �⣺��1����ͼ��֪��a������Ϊ������ƿ��Ũ���������Ϊ���������е�ˮ��������������������ʴ�Ϊ��������ƿ�����������е�ˮ�������������������
��2����Һ©��������һ��ʱ����ٶ�Cװ�ü��ȣ�����������Ŀ�����ų���ϵ�ڵĿ�������ֹ����ʵ�飬��ֹ��ը����Ӧһ��ʱ���D�б�����E����Һ����ǣ�C�з�����Ӧ�Ļ�ѧ����ʽΪFeCO3+H2$\frac{\underline{\;\;��\;\;}}{\;}$Fe+CO2+H2O��
�ʴ�Ϊ���ų���ϵ�ڵĿ�������ֹ����ʵ�飬��ֹ��ը��FeCO3+H2$\frac{\underline{\;\;��\;\;}}{\;}$Fe+CO2+H2O��
��3����Ӧ�����۲쵽Bװ�������ݲ������죬��Ӧ���еIJ����ǵ���A�з�Һ©����������������μ��ٶȣ�
�ʴ�Ϊ������A�з�Һ©����������������μ��ٶȣ�
��4���������м���������ͭ�ٵ�����Zn��Ӧ����Ӧ�������Լӿ죬ԭ����п������ͭ��Ӧ����ͭ��ͭ��п�γ�ԭ��أ�пΪ���������ӿ��˷�Ӧ���ʣ�
�ʴ�Ϊ��п������ͭ��Ӧ����ͭ��ͭ��п�γ�ԭ��أ�пΪ���������ӿ��˷�Ӧ���ʣ�
��5������̼�������к�����Ԫ�ص�ʵ�鷽����ȡ����FeCO3������������ȫ�ܽ⣬�ټ�������K3[Fe��CN��3]��Һ��������ɫ��������̼�������к�����Ԫ�أ�
�ʴ�Ϊ��ȡ����FeCO3������������ȫ�ܽ⣬�ټ�������K3[Fe��CN��3]��Һ��������ɫ��������̼�������к�����Ԫ�أ�
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ�ʵ��װ�á����ʵ����ʼ������ķ�ӦΪ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ����ѧ��Ӧԭ����ʵ��Ľ�ϣ���5��Ϊ�����ѵ㣬��Ŀ�ѶȲ���

 �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д�| A�� | Kspֻ�����ܵ���ʵ����ʺ��¶��йأ�������Һ�е�����Ũ���� | |
| B�� | ��֪ʱ25��ʱKsp[Fe��OH��3]=4.0��10-38������¶��·�ӦFe��OH��3+3H+?Fe3++3H2O��ƽ�ⳣ��K=4.0��104 | |
| C�� | ������Na2SO4��Һ���뵽����ʯ��ˮ�У��а�ɫ����������˵��Ksp[Ca��OH��2]����Ksp��CaSO4�� | |
| D�� | ��֪25��ʱ��Ksp[Mg��OH��2]=1.8��10-11����MgCl2��Һ�м��백ˮ�����Һ��pH=11���������������ʱ��Һ�е�c ��Mg2+��=1.8��10-5mol/L |

 ��
�� ��֪X��Y��Z��M��G�����ֶ���������Ԫ�أ���ԭ��������������Xԭ�Ӻ���ֻ��1�����ӣ�Y��ԭ������������������Ӳ�����2����Y��Gͬ���壻Z��һ�ֵ����������������к��������ߣ�M�ǵؿ��к�����ߵĽ���Ԫ�أ�
��֪X��Y��Z��M��G�����ֶ���������Ԫ�أ���ԭ��������������Xԭ�Ӻ���ֻ��1�����ӣ�Y��ԭ������������������Ӳ�����2����Y��Gͬ���壻Z��һ�ֵ����������������к��������ߣ�M�ǵؿ��к�����ߵĽ���Ԫ�أ� ԭ���������������A��B��C��D��E��F����Ԫ�أ�����A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������A ԭ�ӵ���ͬ��DΪ������������ԭ�Ӱ뾶��������Ԫ�أ�E��Cλ��ͬһ���壬F�� ԭ������Ϊ29��
ԭ���������������A��B��C��D��E��F����Ԫ�أ�����A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��еĵ�������ȣ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������A ԭ�ӵ���ͬ��DΪ������������ԭ�Ӱ뾶��������Ԫ�أ�E��Cλ��ͬһ���壬F�� ԭ������Ϊ29��
 ��һ���¶��£�4L�ܱ�������ijһ��Ӧ������M������N�����ʵ�����ʱ��仯��������ͼ��
��һ���¶��£�4L�ܱ�������ijһ��Ӧ������M������N�����ʵ�����ʱ��仯��������ͼ��
 ����R��R�䡢R���������������ȣ�
����R��R�䡢R���������������ȣ�
 ������F������ͬ�����ŵ�ͬ���칹�干5�֣�����˳���칹��������F����
������F������ͬ�����ŵ�ͬ���칹�干5�֣�����˳���칹��������F���� ����Ӧ����Ϊ��ȥ��Ӧ��
����Ӧ����Ϊ��ȥ��Ӧ��