题目内容
2. 在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:
在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:(1)比较t2时刻,正逆反应速率大小V正>V逆.(填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻用M的浓度变化表示的平均反应速率为:0.25mol/(L•min)
(3)t3时刻化学反应达到平衡,反应物的转化率为75%.
分析 (1)根据图可知,在t2时刻气体N的物质的量在减小,M的物质的量在增加,所以反应在向正反应方向进行,此时V正>V逆;
(2)根据v=$\frac{△c}{△t}$计算反应速率;
(3)根据图可知,从反应开始N的物质的量在减小,所以N为反应物,根据转化率=$\frac{消耗量}{起始量}$×100%计算.
解答 解:(1)根据图可知,在t2时刻气体N的物质的量在减小,M的物质的量在增加,所以反应在向正反应方向进行,此时V正>V逆,
故答案为:>;
( 2)根据v=$\frac{△c}{△t}$计算得M的平均化学反应速率为$\frac{\frac{4mol-2mol}{4L}}{2min}$mol/(L•min)=0.25mol/(L•min),故答案为:0.25mol/(L•min);
(3)根据图可知,从反应开始N的物质的量在减小,所以N为反应物,根据转化率=$\frac{消耗量}{起始量}$×100%计算得N的转化率为$\frac{8mol-2mol}{8mol}$×100%=75%,
故答案为:75%.
点评 本题主要考查化学平衡的相关计算,为高频考点,侧重考查化学反应速率的计算、转化率的计算、影响化学反应速率的因素等知识点,难度不大,解题时注意基础知识的灵活运用.

练习册系列答案
相关题目
13.环境污染与资源短缺问题日趋突出,高效循环利用资源显得尤为重要.工业上用含有Cu2O、Al2O3、Fe2O3和SiO2的矿渣提取铜的工艺流程如图:

已知:①Cu2O+2H+=Cu+Cu2++H2O
②几种氢氧化物开始沉淀和完全沉淀的pH如表:
回答下列问题:
(1)固体A 主要由两种物质组成,其化学式为SiO2、Cu.
(2)酸浸、过滤后,滤液中铁元素的存在形式为Fe2+(填离子符号),生成该离子的离子方程式为2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B的化学式为Fe(OH)3,氧化过程中发生反应的离子方程式为2Fe2++ClO-+2CO32-+3H2O=Fe(OH)3↓+Cl-+2CO2↑.
(4)加NaOH调节溶液pH的范围是5.2≤pH<5.4,工业上对沉淀B、沉淀C的利用应采取的处理方法是加热分解得到相应的氧化物,用于冶炼铁和铝.

已知:①Cu2O+2H+=Cu+Cu2++H2O
②几种氢氧化物开始沉淀和完全沉淀的pH如表:
| 氢氧化物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀的pH | 4.0 | 5.8 | 1.1 | 5.4 |
| 完全沉淀的pH | 5.2 | 8.8 | 3.2 | 6.7 |
(1)固体A 主要由两种物质组成,其化学式为SiO2、Cu.
(2)酸浸、过滤后,滤液中铁元素的存在形式为Fe2+(填离子符号),生成该离子的离子方程式为2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B的化学式为Fe(OH)3,氧化过程中发生反应的离子方程式为2Fe2++ClO-+2CO32-+3H2O=Fe(OH)3↓+Cl-+2CO2↑.
(4)加NaOH调节溶液pH的范围是5.2≤pH<5.4,工业上对沉淀B、沉淀C的利用应采取的处理方法是加热分解得到相应的氧化物,用于冶炼铁和铝.
 纳米级Fe粉是新型材料,具有超强磁性、高效催化性.某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉.其实验设计如图(加热、支持装置省略)
纳米级Fe粉是新型材料,具有超强磁性、高效催化性.某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉.其实验设计如图(加热、支持装置省略)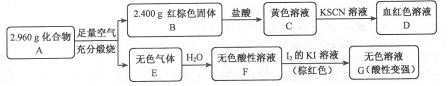
 .写出该反应的离子方程式Fe3S4+6H+=3Fe2++S+3H2S↑.
.写出该反应的离子方程式Fe3S4+6H+=3Fe2++S+3H2S↑.



 .
. .
. .
. .
. .
.