题目内容
胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式: .
考点:钠的重要化合物
专题:元素及其化合物
分析:碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳,据此解答.
解答:
解:胃酸的主要成分为盐酸,盐酸能够与碳酸氢钠发生反应,离子方程式为:H++HCO3-=H2O+CO2↑;
故答案为:H++HCO3-=H2O+CO2↑.
故答案为:H++HCO3-=H2O+CO2↑.
点评:本题考查了碳酸氢钠的性质,明确碳酸氢钠的性质,掌握离子方程式书写的方法和注意事项是解题关键,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g)?cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是( )
| A、平衡正移 |
| B、(a+b)>(c+d) |
| C、Z的体积分数变小 |
| D、X的转化率变大 |
乙烯能够在一定条件下与下列物质发生化学反应的是( )
①水 ②氢气 ③溴水 ④乙烯 ⑤与氯化氢 ⑥酸性高锰酸钾.
①水 ②氢气 ③溴水 ④乙烯 ⑤与氯化氢 ⑥酸性高锰酸钾.
| A、全部 | B、②③⑤ |
| C、①③⑤⑥ | D、②③⑤⑥ |
某气体物质,经测定其蒸气密度折合成标准状况约为1.518 g/L.该化合物可能是下列的( )
| A、HCl |
| B、H2S |
| C、CH4 |
| D、C2H6 |
某温度下,在一容积可变的恒压密闭容器里,反应3A(g)?B(g)+3C(g)达到平衡时,A、B、C的物质的量分别是6mol,2mol,6mol.在保持温度和压强不变的条件下,下列说法正确的是( )
| A、充入1mol的He(He与容器里的气体不反应),平衡不移动 |
| B、充入A、B、C各2mol,平衡将向正反应方向移动 |
| C、将A、B、C各减少1mol,达平衡后C的百分含量增加 |
| D、加入一定量的A气体达平衡后,C的百分含量一定增加 |
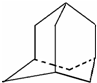 烃A分子的立体结构如图(其中C、H原子已略去);
烃A分子的立体结构如图(其中C、H原子已略去);