题目内容
13g Zn与50mL盐酸恰好完全反应。(1)求在标准状况下产生氢气的体积。
(2)求这种盐酸的物质的量浓度。
(3)若已知该盐酸10mL在该温度条件下其质量为11.3g,求盐酸的质量分数。
答案:
解析:
解析:
| (1)n(Zn)= 由:Zn+2HCl====ZnCl2+H2↑
n( V(H2)=0.2mol×22.4L·mol-1=4.48L。 (2)确定HCl的物质的量,然后计算浓度。 n(HCl)= (3)要确定盐酸的质量分数,必须先确定该盐酸的密度。 ρ(HCl)= ω(HCl)=
|

练习册系列答案
相关题目
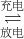 x Mg+Mo3S4,放电时负极反应式为:Mo3S42x--2x e-═Mo3S4
x Mg+Mo3S4,放电时负极反应式为:Mo3S42x--2x e-═Mo3S4